

Auswirkungen von Kupfereinträgen im Weinbau auf die Regenwurmzönose – Ergebnisse von Feldbeprobungen
Effects of copper contamination in viti culture on earthworm cenosis – results of field surveys
Journal für Kulturpflanzen, 65 (12). S. 440–465, 2013, ISSN 1867-0911, DOI: 10.5073/JfK.2013.12.01, Verlag Eugen Ulmer KG, Stuttgart
Nach einer 2009 begonnenen Erhebung zu den Kupfergehalten in der obersten, 20 cm umfassenden Bodenschicht der wichtigsten deutschen Qualitätsweinbaugebiete, über die bereits von Riepert et al., 2010, und Strumpf et al., 2011 und 2012a, berichtet wurde, erfolgte eine umfangreiche Erhebung zur Wirkungsabschätzung an Regenwürmern auf Populationsebene. In einer Machbarkeitsstudie wurde eine vorbereitende Erhebung an jeweils 4 Standorten in jeweils 2 ökologisch wirtschaftenden Betrieben im Herbst 2010 und Frühjahr 2011 durchgeführt. Die dabei berücksichtigten Anbaugebiete schließen Rheinland-Pfalz, Rheinhessen sowie Baden und die Mosel ein. Bestimmend für die Auswahl waren neben den Cu-Gesamtgehalten, Bodeneigenschaften, denen eine wichtige Rolle bei der Verfügbarkeit des Kupfers zugemessen wird. Je Betrieb wurden im Regelfall 3 Versuchsglieder, eine in Bewirtschaftung befindliche Fläche (Prüffläche), eine möglichst niemals genutzte Fläche (Kontrolle) und eine ehemals genutzte Fläche (Referenz) einbezogen. Je Versuchsglied wurden 4 × 0,25 m2, verteilt über den Schlag, per Handauslese und Formalinextraktion gemäß den Vorgaben nach DIN ISO 11266-1 beprobt.
Als Ergebnis der Freilanduntersuchung hat sich herausgestellt, dass die Gesamtabundanzen (Anzahl Würmer über alle Arten) bei niedriger und mittlerer Kupferbelastung wenig aussagekräftig sind und streuungsbedingt Mittelwertvergleiche zu keinen signifikanten Unterschieden führen. Bei näherer Betrachtung der Verteilung auf Lebensformen und bei Betrachtung der Artenzahlen werden dagegen Auswirkungen erkennbar. In der Mehrzahl der untersuchten Flächen reichte eine Auftrennung nach Lebensform aus, um Effekte sichtbar zu machen. Für die verschiedenen Beprobungsflächen berechnete Diversitätsindizes nach Shannon-Wiener bestätigen diese Beobachtungen. Zu beiden Beprobungsterminen, Herbst 2010 und Frühjahr 2011 besteht eine negative Beziehung zwischen Kupfergehalt im Boden und dem Diversitätsindex. Fasst man die beobachteten Auswirkungen auf die Abundanz unter Berücksichtigung statistischer Gesichtspunkte zusammen, so finden sich signifikante Unterschiede zwischen den Abundanzen der Prüf- und Referenzflächen einerseits und den Kontrollflächen andererseits – mit einer Ausnahme – nur bei Flächen mit Cu-Gesamtgehalten > 100 mg Cu/kg und am häufigsten beim Lebensformtyp endogäisch lebende Arten. Dieses Ergebnis wird von einer Diskriminanzanalyse zu den Hauptstreuungsfaktoren unterstützt, wonach Kupfer als maßgebliche Einflussgröße hiernach nur bei den endogäischen Arten eine entscheidende Rolle bei der Abundanzausprägung spielt. Bei den anderen zwei Lebensformtypen sind es eher Bodenparameter wie die Textur oder die Nährstoffversorgung.
Durch die Bestimmung interner Kupfergehalte der aus der Beprobung ins Labor transferierten Würmer können Anhaltspunkte zum Aufnahmeverhalten gewonnen werden. Danach ist die Aufnahmehöhe abhängig von den Cu-Gehalten im Boden. Hinweise auf eine Bioakkumulation im Wurmkörper fehlen. Die Höhe der Aufnahme ist zudem für die drei Lebensformen unterschiedlich, wobei sich die anezischen Arten, gefolgt von den epigäischen Arten, am meisten anzureichern scheinen. Die für die drei Lebensformen unterschiedliche Anreicherung fiel darüber hinaus für die beiden Beprobungszeitpunkte verschieden aus, mit deutlich besserer Korrelation von Boden- und internen Körpergehalten im Herbst 2010.
Eine abschließende Analyse der Auswirkungen von Kupferbelastungen in Qualitätsweinanbaugebieten Deutschlands auf die standorttypische Regenwurmlebensgemeinschaft kann erst nach Vorlage der Ergebnisse aus derzeit laufenden Projekten vorgelegt werden. Die schon jetzt mögliche Interpretation der beobachteten Effekte deutet aber auf Auswirkungen auf Populationsebene bereits ab 100 mg Cu/kg Boden (TM) hin. Es bleibt einer Nutzen-Risikoanalyse überlassen, welche Folgen sich hieraus für das Schutzziel eines nachhaltigen Weinanbaus ergeben.
Stichwörter: Weinbau, Bodenbelastung, Kupfergesamtgehalte, Auswirkungen auf Regenwürmer
On the basis of a survey that had been initiated in 2009 to assess the copper content in the upper 20 cm soil layer in the main wine culturing regions of Germany upon which already has been reported (Riepert et al., 2010, and Strumpf et al., 2011 and 2012a), a comprehensive sampling project was designed to assess the effects on earthworms on population level. It was decided to perform a pre-survey with 8 wine growing farms were selected for a field survey of effects on earthworm populations on cultured sites of organic farming. The design of the survey included besides load aspects also aspects of bio-availability by including a broad range of soil specific parameters. Sampling periods were chosen according to the activity periods of earthworms relevant for our climate zone and resulted in a sampling schedule comprising 4 farms in autumn 2010 and 4 in spring 2011. At each farm typically 3 sites, one under cultivation, one at best without any cultivation (control) and one that had been cultivated in the past but without cultivation in the last 10 years, with copper loads similar to that on the site under cultivation at present (reference). In each treatment group 4 × 0.25 m2 soil samples, regularly distributed over the trial site, earthworms were extracted by means of hand sorting and formalin extraction according to DIN ISO 11266-1.
The evaluation of the extraction indicated that total abundance was a rather insensitive parameter at low and medium copper loads and comparisons of means didn’t result in significant differences of abundance between control and testing site due to the high variation between replicates. Comparing abundance attributed to ecological life forms or species diversity revealed effects instead. In the majority of the assessed sites an evaluated on the level of ecological life forms was sufficient to detect effects. Diversity indices (Shannon-Wiener) that have been calculated for the different types of field sites included in the survey are consistent with these observations. At both extraction periods, in autumn 2010 and spring 2011, a negative correlation was found between the total copper content in soil and the diversity index determined. Summarizing the effects on abundance by taking into account statistical aspects, significant differences in the abundance of earthworms found on testing and reference fields on one hand and control sites on the other hand were observed at Cu-concentrations > 100 mg Cu/kg soil dry mass and most frequently with endogeic species. This result is supported by results of a discriminant analysis on the main factors of variance, revealing that copper is only playing a major role in the variance of abundance for endogeic worms. For the other life forms factors like site specific soil characteristics or nutrient supply seem to play a more important role.
By analysing the internal copper contents in worms that had been transferred from the field site into the laboratory, first information was gained on the uptake behaviour. According to these data the height of uptake depends on the copper concentration in soil but without indicating any bioaccumulation. The intensity of uptake seems to be different for the three life forms, with highest accumulation at anecic worms followed by epigeic worms. The different accumulation observed for the life forms in addition differed between the two extraction periods indicating a much better correlation of soil and body burdens in data gained with the autumn extraction in 2010.
A definitive analysis of the effects of copper load in quality vine growing regions of Germany on site specific earthworm communities cannot be given before the results of the ongoing projects are presented. Interpreting the data available, clear evidence is given for effects on population level at a concentration level of 100 mg Cu/kg (DW) soil. It will be up to a benefit-risk analysis, what consequences have to be drawn with respect to sustainable wine culturing.
Key words: Viniculture, soil contamination, total copper load, effects on earthworms
Kaum ein anderer Pflanzenschutzmittelwirkstoff als Kupfer (Cu2+) hat es geschafft, mehr als 100 Jahre ununterbrochen erfolgreich gegen Pflanzenkrankheiten, wie den Falschen Mehltau an Weinrebe und Hopfen oder die Kraut- und Knollenfäule an Kartoffel, angewendet zu werden. Kupfer wurde dank seiner Bedeutung für verschiedene Kulturen und fehlender Ersatzmittel im Ökologischen Landbau daher auch von der EU-Kommission in Anhang I der Richtlinie 91/414/EWG – verbunden allerdings mit Fristsetzung auf November 2016 und Auflagen – aufgenommen (Backhaus, 2011). Da es sich bei Kupfer um ein Element und nicht um eine synthetisch hergestellte Verbindung handelt, kann der Wirkstoff nicht abgebaut werden und reichert sich daher auf den Produktionsflächen insbesondere der Dauerkulturen an. Elementares Kupfer kann mit einer großen Bandbreite von Verbindungen reagieren, weshalb der bei weitem größte Teil des Kupfers im Boden oder in Gewässern rasch an mineralische Partikel gebunden, als unlösliches anorganisches Salz ausgefällt oder an organische Substanz gebunden wird. Diese Prozesse sind komplexer Natur, enden aber schließlich in der Festlegung freier Kupfer2+ Ionen, die als die biologisch wirksame Form gelten. Der größte Anteil des im Boden befindlichen Kupfers ist deshalb nicht bioverfügbar (DAR, 2003, auszugsweise).
Auswirkungen solcher Alterungsprozesse von Kupferbelastungen haben im Experiment zu 8-fach höheren Wirkungsschwellen bei Regenwürmern im Vergleich mit frisch zudotierten Gehalten geführt (Scott-Fordsmand et al., 2000). Die Übertragung von Schwellenwerten aus Laborversuchen auf Freilandbedingungen im Sinne einer Risikobetrachtung wird dadurch erheblich erschwert. Aussagekräftiger sind daher Freilandbeobachtungen an ausgewählten Indikatororganismen wie z.B. Regenwürmern.
Über die Auswirkungen von kupferhaltigen Pflanzenschutzmitteln und Einträgen aus anderen kupferhaltigen Quellen in der Landwirtschaft auf Bodenorganismen existiert eine umfangreiche Literatur. Übersichten finden sich in Literaturauswertungen bei Jänsch und Römbke (2008) und Riepert (2009). Aus den Untersuchungen lässt sich ableiten, dass Kupfer bei langjähriger Anwendung schädigend auf viele Arten von Bodenorganismen wirkt. Aufgrund unterschiedlicher artspezifischer Empfindlichkeit gegenüber Kupfer kann es zur Verschiebung des Artengefüges auf kupferbelasteten Standorten kommen. Insgesamt sinkt die Biodiversität mit steigendem Kupfergehalt. Anpassungsmechanismen an erhöhte Kupferkonzentrationen sind je nach Art in Abhängigkeit vom Vorhandensein von Entgiftungsmechanismen möglich. Neben dem Kupfergehalt wirken sich auch andere Bewirtschaftungsfaktoren mit Wirkung auf die Nährstoffzufuhr und Feuchteregulierung des Bodens auf Abundanz, Biomasse und Artenvielfalt im Boden aus Riepert (2009).
Die von der EU-Kommission mit der Aufnahme von Kupfer in den Anhang I festgelegten Auflagen betreffen daher auch die Ergreifung von Maßnahmen zur Reduzierung der Aufwandmengen und Lieferung aktueller Monitoringdaten zu unerwünschten Auswirkungen.
Neben den Prüfanforderungen, die sich aus diesen Auflagen für Antragsteller im Rahmen des Zulassungsverfahrens für Pflanzenschutzmittel ergeben, wurde in mehreren Fachgesprächen zwischen Ministerien, Behörden, Anbauverbänden und beteiligten Kreisen der Bedarf an repräsentativen Daten zu den Kupfergehalten auf relevanten Anbauflächen formuliert. In den Jahren 2009–2010 wurden vom, Julius Kühn-Institut – Bundesforschungsinstitut für Kulturpflanzen (JKI), als Ergebnis zwischenbehördlicher Abstimmung Beprobungen zur Beschreibung der aktuellen Situation der Kupferbelastung in Weinbergsböden durchgeführt (Strumpf et al., 2011). Die im Verlaufe dieser Erhebungen gewonnenen Daten zu Gehalten in der oberen Bodenschicht bis 20 cm Tiefe sowie zur Beschreibung der Bodengüte und Bewirtschaftungsweise hatten die Voraussetzung für eine in den Jahren 2010 und 2011 an jeweils 4 Betrieben vorgenommenen Erhebung zur Erfassung des Zustandes von Regenwurmzönosen geschaffen.
Zielsetzung dieser Erhebungen war die Prüfung methodischer Aspekte für die Erarbeitung von Hinweisen zur Erteilung von Vorgaben späterer Monitoringuntersuchungen im Zuge des Zulassungsverfahrens von Pflanzenschutzmitteln und die Identifizierung derjenigen Faktoren, die Einfluss auf Abundanz und Artenvielfalt der örtlichen Regenwurmzönose nehmen. Begleitet wurden diese Erhebungen von standardisierten Laborversuchen an mitgenommenen Bodenproben für chemisch-analytische Untersuchungen, bodenkundliche Bestimmungen und zur biologischen Charakterisierung der Bodenproben. Berichte über vorläufige Ergebnisse der Labor- und Freilandversuche finden sich in Riepert et al., 2012a und 2012b, Felgentreu et al., 2012 und Strumpf et al., 2012b.
Auf der Grundlage der 2009 begonnenen Erhebung zum Kupfergehalt in der belebten Bodenschicht bis 20 cm Tiefe in den Hauptsonderkulturen Wein-, Obst- und Hopfenbau konnten unter Berücksichtigung der breiten Spanne der bestimmten Kupfergesamtgehalte (s. Tab. 3) auf den Bewirtschaftungsflächen und anderer wichtiger Bodenkenngrößen der Stichprobe insgesamt 8 Betriebe (s. Tab. 2) für eine Freilandbeprobung der Regenwurmlebensgemeinschaft im Ökologischen Weinbau ausgewählt werden. Bestimmend für die Auswahl waren neben den Cu-Gesamtgehalten Bodeneigenschaften, denen eine wichtige Rolle bei der Verfügbarkeit des Kupfers zugemessen wird. Da Beprobungen nur während der Aktivitätsphasen von Regenwürmern, in unseren Breiten im Frühjahr und im Herbst, sinnvoll sind, wurde die Beprobung von jeweils 4 Betrieben auf den Herbst 2010 und das Frühjahr 2011 gelegt. Je zwei Betriebe fielen dabei auf die Anbaugebiete Pfalz, Rheinhessen sowie Mittelmosel und Baden. Je Betrieb wurden im Regelfall 3 Versuchsglieder, eine in Bewirtschaftung befindliche Fläche (Prüffläche), eine möglichst niemals weinbaulich genutzte Fläche (Kontrolle) und eine ehemals weinbaulich genutzte Fläche (Referenz) einbezogen. Letztere Fläche dient der Einschätzung des Einflusses von Bewirtschaftungsmaßnahmen wie z.B. der Bodenbearbeitung oder der Düngung. Je Versuchsglied wurden 4 × 0,25 m2, verteilt über den Schlag, per Handauslese und Formalinextraktion gemäß den Vorgaben nach DIN ISO 23611-1 beprobt. Die ausgelesenen Würmer wurden getrennt nach Versuchsglied in Kunststoffbehältern in Kühlboxen zwischengelagert und möglichst zeitnah zur taxonomischen Bestimmung im Labor per Expresslieferung versandt. Je Beprobungsstelle wurden Bodenproben für die spätere Elementanalytik und für die Bestimmung der wichtigsten bodenkundlichen Parameter entnommen (Abb. 1a bis 1e).
Tab. 3. Kupfergehalte und bestimmte Bodenparameter (Mittelwerte aus 4 Beprobungsstellen je 0.25 m2 des jeweiligen Prüfgliedes) im Oktober 2010 und im April 2011
Betrieb | Prüfglied1) | Cu | pH | org. S | Sand | Schluff | Ton | Corg | N | C/N |
[mg/kg] | [%] | |||||||||
Oktober 2010 | ||||||||||
PF02 | KO | 47,50 | 7,58 | 8,60 | 12 | 66 | 22 | 4,28 | 0,20 | 8,75 |
PF | 74,25 | 7,58 | 12,10 | 23 | 50 | 26 | 6,03 | 0,20 | 12,25 | |
RF | 49,25 | 7,65 | 11,60 | 20 | 42 | 38 | 5,80 | 0,17 | 11,75 | |
PF03 | KO | 28,50 | 7,60 | 7,70 | 31 | 52 | 18 | 3,84 | 0,15 | 7,75 |
PF | 179,00 | 7,58 | 5,10 | 17 | 65 | 17 | 2,55 | 0,17 | 5,25 | |
RF | 34,25 | 7,68 | 6,20 | 35 | 52 | 12 | 3,09 | 0,09 | 6,25 | |
RH04 | KO | 18,00 | 7,60 | 9,40 | 4 | 32 | 74 | 4,70 | 0,16 | 9,50 |
PF | 133,00 | 7,75 | 10,20 | 16 | 62 | 21 | 5,10 | 0,12 | 10,25 | |
RF | 124,25 | 7,60 | 10,60 | 18 | 57 | 24 | 5,31 | 0,18 | 10,50 | |
RH06 | KO | 25,75 | 7,65 | 6,70 | 9 | 59 | 32 | 3,37 | 0,16 | 6,50 |
PF | 38,00 | 7,73 | 5,20 | 7 | 63 | 30 | 2,60 | 0,17 | 5,50 | |
RF | 107,00 | 7,63 | 8,60 | 14 | 43 | 43 | 4,31 | 0,21 | 8,50 | |
April 2011 | ||||||||||
BA01 | KO | 88,25 | 7,53 | 8,68 | 18 | 44 | 38 | 4,34 | 0,34 | 13,00 |
PF1 | 27,50 | 7,48 | 8,38 | 9 | 67 | 24 | 4,18 | 0,17 | 26,25 | |
PF2 | 225,25 | 7,48 | 8,55 | 20 | 53 | 27 | 4,27 | 0,25 | 18,00 | |
RF | 187,75 | 7,58 | 9,83 | 15 | 69 | 16 | 4,92 | 0,21 | 24,00 | |
BA02 | KO | 25,00 | 7,20 | 5,10 | 7 | 57 | 36 | 2,56 | 0,22 | 12,25 |
PF | 185,75 | 7,35 | 8,13 | 24 | 41 | 35 | 4,08 | 0,28 | 15,25 | |
RF | 305,25 | 7,28 | 9,35 | 26 | 39 | 35 | 4,68 | 0,30 | 16,75 | |
MO03 | KO | 19,50 | 5,63 | 4,83 | 39 | 39 | 22 | 2,42 | 0,25 | 9,50 |
PF1 | 29,00 | 6,25 | 3,90 | 36 | 41 | 23 | 1,97 | 0,27 | 7,50 | |
PF2 | 211,50 | 6,63 | 6,38 | 59 | 23 | 18 | 3,19 | 0,35 | 9,00 | |
RF | 276,00 | 5,33 | 4,70 | 62 | 25 | 13 | 2,36 | 0,25 | 9,00 | |
MO06 | KO | 22,50 | 5,05 | 4,18 | 57 | 26 | 17 | 2,09 | 0,24 | 8,75 |
PF | 227,50 | 6,83 | 6,63 | 56 | 28 | 16 | 3,31 | 0,34 | 9,75 | |
RF | 93,50 | 7,20 | 8,25 | 58 | 29 | 14 | 4,13 | 0,40 | 10,50 | |
1) KO = Kontrolle. PF = Prüffläche. PF2 = zusätzliche Prüffläche. RF = Referenzfläche | ||||||||||
Tab. 2. Kurzcharakterisierung der Beprobungsflächen
Betrieb | Fläche | Bodenart – Flächenbeschreibung | |
RH_04 | Prüffläche | Ul3 | Bewirtschaftung seit mindestens 100 Jahren, Flurbereinigung 1985, ökologischer Anbau seit 1990 |
Referenzfläche | Ltu | Weinbrache seit 1980, keine Flurbereinigung, Sukzession | |
Kontrollfläche | Ul2 | Wiese mit Spontanvegetation (Rand-/Ruderalfläche), neben Ackerflächen | |
RH_06 | Prüffläche | Ltu | Weinbau seit 1976. ökologische Bewirtschaftung; alternierende Begrünung |
Referenzfläche | Lt3 | Weinbrache seit 1999, davor verstärkt Tresteraufbringung, jetzt Grünland, Hanglage 15–20% | |
Kontrollfläche | Ltu | Ackerrandstreifen, gegenüber Prüffläche | |
PF_02 | Prüffläche | Ltu | Bewirtschaftung seit mindestens 100 Jahren, ökologischer Anbau seit 1989, alternierende Begrünung, Hanglage 20% |
Referenzfläche | Lt3 | Weinbrache seit 1989, jetzt verbuschtes Grünland, Hanglage 25% | |
Kontrollfläche | Ltu | Dauergrünland in Hofnähe | |
PF_03 | Prüffläche | Lt2 | Bewirtschaftung seit mindestens 100 Jahren, ökologischer Anbau seit 1980, Untersaatmischung abwechselnd mit Dauerbegrünung, Hanglage 15% |
Referenzfläche | Lsu | Weinbau bis 2000, jetzt Streuobstwiese | |
Kontrollfläche | Lu4 | Dauergrünland | |
BA_01 | Prüffläche 1 | Ltu | Anbau 30 Jahre, ökologischer Anbau seit 1990, Dauerbegrünung |
Prüffläche 2 | Tu | Anbau 50 Jahre, ökologischer Anbau seit 1990, Dauerbegrünung | |
Referenzfläche | Lu4 | Weinbrache seit 1994, Sukzession | |
Kontrollfläche | Tl | Streuobstwiese seit 40 Jahren | |
BA_02 | Prüffläche | Tu | konventioneller Anbau seit 100 Jahren, Hanglage 20–30% |
Referenzfläche | Ltu | Weinbrache seit 2004, beginnende Sukzession, Hanglage 35% | |
Kontrollfläche | Ltu | Wiese, früher 2 Jahre Apfelanbau | |
MO_03 | Prüffläche 1 | Lu | ökologischer Anbau 14 Jahre, Dauerbegrünung |
Prüffläche 2 | Lu | Nutzung seit 100 Jahren, ökologischer Anbau seit 28 Jahren, Dauerbegrünung | |
Referenzfläche | Ls3 | Weinbrache seit 1997, Spontanvegetation | |
Kontrollfläche | Lu | Wiese seit 30 Jahren | |
MO_06 | Prüffläche | Us | Anbau seit mehr als 100 Jahren, ökologischer Anbau seit 7 Jahren |
Referenzfläche | Su3 | Weinbrache seit 2001, jetzt Grünland, Hanglage 50% | |
Kontrollfläche | Sl4 | Streuobstwiese seit 1975 | |

Abb. 1. Beprobungsrahmen aus Aluminium und Kunststoffbehälter zum Sammeln des Aushubs für die anschließende Handauslese.
Die taxonomische Bestimmung bis auf Artebene wurde an lebenden Tieren unter Nutzung der Bestimmungsliteratur von Sims und Gerard (1999), Graff (1953) und Christian und Zicsi (1999) durchgeführt. Die Nomenklatur richtet sich nach Easton (1983). Die identifizierten Arten sind in Tab. 1 zusammengestellt. (Tab. 1, Tab. 2)
Tab. 1. Identifizierte Regenwurmarten (fett: dominante Arten) mit in nachfolgenden Abbildungen verwendeten Kurzbezeichnungen in Klammern
Lebensformen | ||
Streubewohner | Mineralbodenbewohner | Tiefengräber |
Dendrobaena rubida (DRUBI) | Aporrectodea caliginosa (ACALI) | Allolobophora longa (ALONG) |
Dendrobaena octaedra (DOKTA) | Allolobophora chlorotica (ACLO) | Lumbricus terrestris (LTERR) |
Eisenia fetida (EFETI) | Allolobophora icterica (AICTE) | |
Lumbricus rubellus (LRUBE) | Aporrectodea nocturna (ANOCT) | |
Lumbricus castaneus (LCAST) | Aporrectodea rosea (AROSE) | |
Octolasion cyaneum (OCYAN) | ||
Octolasion tyrtaeum (OTYRT) | ||

Abb. 1. Handauslese der streubewohnenden Arten (epigäische Arten) und der Flachgräber (endogäische Arten) unter einem Schutzzelt.
Zur Analyse der Gesamtgehalte in Königswasser (VDLUFA, 1991a) und bodenkundlicher Basisparameter [Korngröße (DIN, 1997; DIN, 2008), pH-Wert (VDLUFA, 1991b), org. Substanz (DIN, 1996), C/N-Verhältnis (DIN, 1998) – Zuordnung der Bodenarten nach DIN 4220] wurden Proben des Bodenaushubs der Regenwurmextraktion im Freiland entnommen und zur weiteren Probenvorbereitung im Labor in das Institut in Berlin-Dahlem transportiert (Tab. 3).
Abundanzbestimmungen.
Als Ergebnis der Freilanduntersuchung im Oktober 2010 hat sich herausgestellt, dass die Gesamtabundanzen (Anzahl Würmer über alle Arten je m2) bei niedriger und mittlerer Kupferbelastung wenig
aussagekräftig sind und streuungsbedingt Mittelwertvergleiche zu keinen signifikanten Unterschieden führen (Abb. 2a). Signifikante Unterschiede zur Kontrolle (p ≤ 0,05) fanden sich nur bei der Referenzfläche von RH_04.
![Abb. 2. Mittlere Gesamtabundanzen [n/m2] der in den 3 Versuchsgliedern Kontrolle (KO), Prüffläche (PF) und Referenzfläche (RF) extrahierten Regenwürmer der im Oktober 2010 beprobten 4 Betriebe in der Pfalz und Rheinhessen.](bilder/riepert_et_al_bld-002a.jpg)
Abb. 2. Mittlere Gesamtabundanzen [n/m2] der in den 3 Versuchsgliedern Kontrolle (KO), Prüffläche (PF) und Referenzfläche (RF) extrahierten Regenwürmer der im Oktober 2010 beprobten 4 Betriebe in der Pfalz und Rheinhessen.
Die Gehalte in den aktuell bewirtschafteten Prüfflächen (fett) decken einen Bereich geringer bis mittelstarker Belastung ab.
Biomassebestimmungen. Ein ähnlich wenig aussagekräftiges Bild ergibt sich beim Vergleich der mittleren Gesamtbiomassen [g/m2] der extrahierten Würmer der jeweiligen Versuchsglieder (Abb. 2b). In keinem Fall konnten statistisch signifikante Unterschiede zur Kontrolle (p ≤ 0,05) gefunden werden.
![Abb. 2. Mittlere Gesamtbiomassen [g/m2] der in den 3 Versuchsgliedern Kontrolle (KO), Prüffläche (PF) und Referenzfläche (RF) extrahierten Regenwürmer der im Oktober 2010 beprobten 4 Betriebe in der Pfalz und Rheinhessen.](bilder/riepert_et_al_bld-002b.jpg)
Abb. 2. Mittlere Gesamtbiomassen [g/m2] der in den 3 Versuchsgliedern Kontrolle (KO), Prüffläche (PF) und Referenzfläche (RF) extrahierten Regenwürmer der im Oktober 2010 beprobten 4 Betriebe in der Pfalz und Rheinhessen.
Abundanzbestimmungen. Bei der Beprobung im Frühjahr 2011 in den Weinanbaugebieten Badens und der Mosel waren Betriebe mit einer Spanne von Gesamtgehalten ausgewählt worden, die auf den Prüfflächen zwischen 27 und 227 mg Cu/kg Boden TM reichte. Insbesondere bei den Betrieben an der Mosel fielen die Abundanzunterschiede in der Tendenz und auch statistisch klarer aus. Statistisch signifikant (p ≤ 0,05) verschieden zur Kontrolle waren die Prüfglieder PF und RF von BA_02, PF_2 und RF von MO_03. Trotz deutlicher Unterschiede bei den Mittelwerten waren die Unterschiede der Abundanzen auf den beprobten Flächen von MO_06 nicht signifikant (Abb. 3a). Angesichts der hohen Gehalte in den Prüfflächen aller untersuchten Betriebe war jedoch ein klareres Ergebnis erwartet worden.
![Abb. 3. Mittlere Gesamtabundanzen [n/m2] der in den 3 Versuchsgliedern (zweimal musste wegen der sehr geringen Kupferbelastung in der ausgewählten Prüffläche eine weitere Prüffläche (PF2) hinzugezogen werden), Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF) extrahierten Regenwürmer der im April 2011 beprobten 4 Betriebe Badens und an der Mosel.](bilder/riepert_et_al_bld-003a.jpg)
Abb. 3. Mittlere Gesamtabundanzen [n/m2] der in den 3 Versuchsgliedern (zweimal musste wegen der sehr geringen Kupferbelastung in der ausgewählten Prüffläche eine weitere Prüffläche (PF2) hinzugezogen werden), Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF) extrahierten Regenwürmer der im April 2011 beprobten 4 Betriebe Badens und an der Mosel.
Die Gehalte in den aktuell bewirtschafteten Prüfflächen (fett) decken einen Bereich geringer bis starker Belastung ab.
Biomassebestimmungen. Statistisch signifikante Unterschiede zur Kontrollfläche zwischen den mittleren Gesamtbiomassen traten bei der 2. Prüffläche und auch bei der Referenzfläche des Betriebs MO_03 auf. Auf beiden Flächen wurden mittlere Cu-Gesamtgehalte von 212 bzw. 276 mg Cu/kg Boden TM bestimmt. Beim Betrieb MO_06 ist lediglich die mittlere Gesamtbiomasse der extrahierten Würmer der Referenzfläche (93 mg Cu/kg Boden TM) signifikant verschieden von der Biomasseentwicklung der Würmer der Kontrollfläche. In der Tendenz entspricht die Biomasseentwicklung erwartungsgemäß der Abundanzentwicklung (Abb. 3b).
![Abb. 3. Mittlere Gesamtbiomassen [g/m2] der in den 3 Versuchsgliedern (zweimal musste wegen der sehr geringen Kupferbelastung in der ausgewählten Prüffläche eine weitere Prüffläche (PF2) hinzugezogen werden), Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF) extrahierten Regenwürmer der im April 2011 beprobten 4 Betriebe Badens und an der Mosel.](bilder/riepert_et_al_bld-003b.jpg)
Abb. 3. Mittlere Gesamtbiomassen [g/m2] der in den 3 Versuchsgliedern (zweimal musste wegen der sehr geringen Kupferbelastung in der ausgewählten Prüffläche eine weitere Prüffläche (PF2) hinzugezogen werden), Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF) extrahierten Regenwürmer der im April 2011 beprobten 4 Betriebe Badens und an der Mosel.
Grundsätzlich lassen sich nach Bouché (1977) die drei nachfolgend dargestellten Lebensformtypen differenzieren:
– Streubewohner: Epigäische Regenwurmarten leben vorzugsweise in der Streu- und Humusschicht an der Bodenoberfläche und ernähren sich von Pflanzenresten, Bakterien, Pilzen und Algen. Typische Vertreter: Roter Laubfresser (Lumbricus rubellus), Brauner Laubfresser (Lumbricus castaneus), Köcherwurm (Dendrobaena rubida) und Kompostwurm (Eisenia fetida). |
– Mineralbodenbewohner: Endogäische Regenwurmarten leben in horizontalen Gängen und ernähren sich von abgestorbenen Wurzeln (rhizophag) und organischen Substanzen im Boden (geophag). Typische Vertreter: Kl. Wiesenwurm (Aporrectodea caliginosa), der Kl. Ackerwurm (Allolobophora chlorotica) und der Große Ackerwurm (Octolasium lacteum). |
– Vertikalbohrer/Tiefgräber: anözische bzw. anektische Regenwurmarten bewegen sich zwischen den Bodenschichten vom Mineralboden bis zur Bodenoberfläche. Sie ernähren sich von Blättern und anderen Streuresten an der Bodenoberfläche, die sie in ihre Gänge ziehen, dort auffressen und verdauen. Der Kot wird zur Bodenoberfläche hin ausgeschieden. Typische Vertreter: Tauwurm (Lumbricus terrestris), Großer Wiesenwurm (Aporrectodea longa). |
Beprobungsjahr 2010. Bei näherer Betrachtung der Verteilung der Abundanzen auf Lebensformen (Abb. 4a und 5a) und erst recht bei Betrachtung der Artenzahlen am Beispiel der Betriebe PF_02 und PF_03, werden anders als beim Endpunkt Gesamtabundanz Auswirkungen erkennbar.
Im Betrieb PF_02 mit seiner mäßigen Kupferbelastung auf der Prüffläche ist die Verteilung der Abundanzen auf die Lebensformtypen in allen drei Prüfgliedern sehr ähnlich. Die stets schwach vertretenen epigäischen Arten wurden auf der Prüffläche nicht extrahiert, was angesichts der geringen Zahlen in der Kontrolle wohl nicht der Cu-Belastung zuzuschreiben ist. Bei einer Verfeinerung der Analyse (Abb. 4b) zeigt sich allerdings, dass auch die Prüffläche des Betriebs PF_02 auf der Ebene der Arten von einer Reduktion betroffen ist, obwohl die Gesamtabundanz endogäisch lebender Regenwürmer noch nicht betroffen ist.
![Abb. 4. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb PF_02 (Kupfergesamtgehalte s. neben Abb. 4a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-004b.jpg)
Abb. 4. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb PF_02 (Kupfergesamtgehalte s. neben Abb. 4a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.
Anders stellt sich das Bild beim Betrieb PF_03 dar, der mit 179 mg Cu/kg Boden TM schon eine deutlich erhöhte Belastung aufweist. Hier ist der Anteil endogäischer Arten auf der Prüffläche gegenüber den beiden anderen Prüfgliedern mit geringerer Belastung stark reduziert und verhilft den Tiefengräbern zu einem überproportional hohen relativen Anteil (Abb. 5a).
Für den Betrieb PF_03 gilt die bereits bei PF_02 beobachtete Dominanzverschiebung noch stärker (Abb. 5b). Anstelle der endogäisch lebenden Würmer dominiert mit einem Anteil von 91% der Tiefengräber L. terrestris.
![Abb. 5. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb PF_03 (Kupfergesamtgehalte s. neben Abb. 5a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-005b.jpg)
Abb. 5. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb PF_03 (Kupfergesamtgehalte s. neben Abb. 5a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.
Die Gesamtabundanzen der beprobten Flächen von Betrieb RH_04 sind insofern unerwartet, als der niedrigste Mittelwert auf der Kontrollfläche bestimmt wurde, obwohl hier mit 18 mg Cu/kg Boden TM ein sehr geringer Gehalt gemessen wurde. Sowohl die Prüf- als auch die Referenzfläche mit 133 bzw. 124 mg Cu/kg Boden TM weisen erhöhte Kupfergehalte auf, haben aber höhere mittlere Abundanzen (99 bzw 158 Ind./m2) gegenüber 74 Ind./m2 in der Kontrolle. Die Abundanzanteile je Lebensformtyp (Abb. 6a) zeigen aber bei der Prüffläche ein deutliches Absinken des Anteils endogäischer Arten. Dies gilt jedoch nicht für die Referenzfläche, die bei ähnlich hohem Kupfergehalt eine der Kontrollfläche ähnliche Verteilung der Abundanzanteile aufweist. Da die Referenzfläche seit 1980 nicht mehr in Nutzung steht, könnten auch andere Faktoren wie beispielsweise die Bodenbearbeitung auf der Prüffläche eine Rolle bei der Abundanzausprägung spielen. Die als Kontrolle herangezogene Ruderalfläche neben ackerbaulicher Nutzung könnte ebenfalls von Bewirtschaftungseinflüssen betroffen sein. Die Verteilung der Abundanzen auf die extrahierten Arten (Abb. 6b) zeigt, dass üblicherweise dominante endogäische Arten wie A. caliginosa in allen Versuchsgliedern fehlen und durch O. tyrtaeum auf der Kontroll- bzw. Referenzfläche ersetzt werden. Die Abundanz auf der Prüffläche wird vom Tiefengräber L. terrestris bestimmt.
Insgesamt war die Artenzahl in allen Prüfgliedern eher gering.
![Abb. 6. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb RH_04 (Kupfergesamtgehalte s. neben Abb. 6a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-006b.jpg)
Abb. 6. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb RH_04 (Kupfergesamtgehalte s. neben Abb. 6a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.
Die Abundanzen des Betriebes RH_06 geben bei der Zuordnung der Ursachen ebenso Rätsel auf, als hier die Prüffläche einen ähnlich geringen Kupfergehalt von 38 mg Cu/kg Boden TM wie die Kontrolle mit 26 mg Cu/kg Boden TM aufweist, während die Referenzfläche mit 107 mg Cu/kg Boden TM deutlich über diesen Werten liegt. Der höchste Abundanzmittelwert findet sich jedoch bei der Referenzfläche, ohne statistisch signifikant verschieden von den beiden anderen Mittelwerten aus Prüffläche und Kontrolle zu sein. Aus der Verteilung auf die Lebensformtypen (Abb. 7a) lässt sich lediglich bei der Prüffläche ein geringfügig verringerter Anteil endogäischer Würmer erkennen. Abb. 7b zeigt, dass sich die Artenzahl der Referenzfläche mit dem höchsten Kupfergehalt der drei Flächen auf eine endogäische Art A. chlorotica und auf eine anezische Art, L. terrestris beschränkt. Insgesamt ist das Artenspektrum eher als schmal zu bezeichnen. Eine eindeutige Zuordnung zu den gemessenen Kupfergehalten ist nicht möglich.
![Abb. 7. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb RH_06 (Kupfergesamtgehalte s. neben Abb. 7a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-007b.jpg)
Abb. 7. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb RH_06 (Kupfergesamtgehalte s. neben Abb. 7a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, INDET = unbestimmte Art.
Beprobungsjahr 2011. Von den 2011 beprobten Betrieben war bereits das Ergebnis bei Betrachtung der Gesamtabundanz wesentlich klarer. Ein Blick auf die Abundanzverteilung auf die Lebensformtypen und die Arten zeigt, dass auch im Betrieb BA_01, der keine signifikanten Unterschiede in der Gesamtabundanz aufwies, Auswirkungen auf die Verteilung sichtbar werden (Abb. 8a).
Auf der Prüffläche, die erst seit 1980 in Nutzung (ökologischer Anbau seit 1990) ist, wurde der niedrigste Cu-Gesamtgehalt gemessen, der damit noch im Bereich üblicher geogener Konzentrationen liegt. Erwartungsgemäß liegt eine Verteilung mit hohem Anteil endogäisch lebender Würmer vor. Auf allen übrigen Flächen, auch auf der Kontrollfläche mit möglicherweise anderer früherer Nutzung ist der Anteil der endogäisch lebenden Arten geringer bzw. sehr gering (Prüffläche 2 und Referenzfläche). Werden die Artenanteile in die Analyse mit einbezogen (Abb. 8b) zeigt sich, dass in der Kontrolle mit mittleren Cu-Gehalten zwar noch ähnlich viele Arten wie auf der Prüffläche (PF) mit dem geringsten Cu-Gehalt (27 mg Cu/kg Boden TM) angetroffen werden, aber normalerweise dominante endogäische Arten wie A. caliginosa und A. rosea fehlen. Ein Effekt, der dann bei den Prüfgliedern PF2 und RF erwartungsgemäß ebenfalls auftritt.
![Abb. 8. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb BA_01 (Kupfergesamtgehalte s. neben Abb. 8a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-008b.jpg)
Abb. 8. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb BA_01 (Kupfergesamtgehalte s. neben Abb. 8a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, INDET = unbestimmte Art.
Beim Betrieb BA_02 hatten die Gesamtabundanzen angesichts der gemessenen hohen Cu-Gehalte von 186 mg Cu/kg Boden TM auf der Prüffläche und 305 mg Cu/kg Boden TM auf der Referenzfläche bereits deutliche Effekte erkennen lassen. Die Verteilung der Abundanzen auf die Lebensformtypen (Abb. 9a) zeigt entsprechend deutlich, dass endogäische Arten nur noch einen Anteil von 5% und 10% an der Gesamtabundanz haben und epigäische Arten gänzlich fehlen. Bei der Referenzfläche handelt es sich um eine Brache, die seit 2004 aus der weinbaulichen Nutzung genommen wurde (Abb. 9b).
![Abb. 9. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb BA_02 (Kupfergesamtgehalte s. neben Abb. 9a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-009b.jpg)
Abb. 9. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb BA_02 (Kupfergesamtgehalte s. neben Abb. 9a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, INDET = unbestimmte Art.
Am Beispiel dieser hoch belasteten Prüf- und Referenzfläche bei BA_02 ist gut die Dominanzverschiebung von den endogäischen Arten A. caliginosa und A. rosea hin zu 2 anezischen Arten, A. longa und L. terrestris, erkennbar.
Beim Betrieb MO_03 mit hohen Kupfergehalten von 212 mg Cu/kg Boden TM auf Prüffläche 2 und 276 mg Cu/kg Boden TM auf der Referenzfläche hatten sich statistisch signifikante Unterschiede bei den Gesamtabundanzen und Gesamtbiomassen im Vergleich zur Kontrollfläche ergeben. Ein Blick auf die Lebensformtypen (Abb. 10a) zeigt, dass in diesem Fall neben den endogäischen auch die anezischen Arten fehlen. Von den epigäischen Arten sind es L. rubellus und L. castaneus sowie auf der Referenzfläche Dendrobaena rubida und die Kompostart Eisenia fetida, die gefunden wurden (s. Abb. 10b).
![Abb. 10. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb MO_03 (Kupfergesamtgehalte s. neben Abb. 10a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, LSPEC = Lumbricus Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-010b.jpg)
Abb. 10. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb MO_03 (Kupfergesamtgehalte s. neben Abb. 10a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, OSPEC = Octolasium Arten, LSPEC = Lumbricus Arten, INDET = unbestimmte Art.
Die Prüffläche des Betriebes MO_06 wies mit 227 mg Cu/kg Boden TM ebenfalls einen hohen Gesamtgehalt auf. Die Referenzfläche hatte mit 93 mg Cu/kg Boden TM einen eher mittleren Gehalt. Auf beiden Flächen wurden zwar verringerte Gesamtabundanzen gefunden, die sich aber statistisch nicht von der Kontrolle unterschieden. Die Abundanzverteilung auf die Lebensformtypen (Abb. 11a) zeigt aber, dass auf der Prüffläche die endogäischen Arten unterrepräsentiert sind. Auf der Referenzfläche wurden zwar weniger Würmer als in der Kontrolle gefunden, die relative Verteilung auf die Lebensformtypen ähnelt jedoch der der Kontrolle. Die Unterschiede bei den identifizierten Arten von Prüf- und Referenzfläche sind eher gering (Abb. 11b).
![Abb. 11. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb MO_06 (Kupfergesamtgehalte s. neben Abb. 11a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, LSPEC = Lumbricus Arten, INDET = unbestimmte Art.](bilder/riepert_et_al_bld-011b.jpg)
Abb. 11. Relativer Anteil [%] der extrahierten Arten an den Abundanzen je Prüfglied im Betrieb MO_06 (Kupfergesamtgehalte s. neben Abb. 11a). Kürzel der Arten s. Tab. 1 und ASPEC = Aporrectodea Arten, LSPEC = Lumbricus Arten, INDET = unbestimmte Art.
Zur Beurteilung der Stabilität einer Taxozönose und für Vergleichszwecke wird als Maß für die Artenvielfalt häufig der Shannon-Wiener-Index H (Spellerberg und Fedor, 2003; Neubert, 2012) verwendet. Neben der reinen Artenzahl berücksichtigt dieser Index auch die relative Häufigkeit oder Dominanz jeder Art,
wobei H ein Ausdruck für die Diversität in einer Gruppe von n Arten ist, n = Anzahl der vorhandenen Arten; pi = relative Abundanz der i-ten Art, gemessen von 0,0–1,0 (gehören 10% der extrahierten Organismen dieser Art an, so ist pi 0,10).
H gibt den Grad der „Ungewissheit“ an. Der kleinste Wert 0 für die Artendiversität ergibt sich, wenn nur eine Art mit 100% am Individuenbestand beteiligt ist. Der Maximalwert (H = Hmax) wird erreicht, wenn die Artenanzahl gleich der Individuenanzahl ist oder bei vorhandener Artenanzahl alle den gleichen Individuenanteil haben (p1 = p2 = p3 …).
Hmax kann mit folgender Formel berechnet werden:
Hmax = –ln(1/i); i = Anzahl der Arten. Das Verhältnis von H zu Hmax wird häufig als Eveness E bezeichnet. Dieser Quotient erreicht die Werte zwischen 0 und 1. Je stärker E von 1 verschieden ist, desto mehr weichen die Dominanzverhältnisse verschiedener Arten von einer Gleichverteilung ab (Bäumler, 2011) (Tab. 4).
Tab. 4. Shannon-Wiener-Index H. Hmax und der Eveness E der Behandlungsgruppen Kontrolle (KO). Prüffläche (PF) bzw. (PF2) und Referenzfläche (RF). der in den Jahren 2010 und 2011 beprobten Betriebe in Rheinland-Pfalz, Rheinhessen, der Mosel und in Baden
Beobachtung | Betrieb | Cu-Gehalt | Beprobungsfläche | H | Hmax | E (H/Hmax) |
2010 | ||||||
1 | PF_02 | 47,50 | KO | 2,28 | 2,40 | 0.95 |
2 | 74,25 | PF | 1,26 | 1,61 | 0.78 | |
3 | 49,25 | RF | 1,98 | 2,20 | 0.90 | |
4 | PF_03 | 28,50 | KO | 2,09 | 2,30 | 0.91 |
5 | 179,00 | PF | 1,29 | 1,39 | 0.93 | |
6 | 34,25 | RF | 2,14 | 2,30 | 0.93 | |
7 | RH_04 | 18,00 | KO | 1,47 | 1,61 | 0.91 |
8 | 133,00 | PF | 1,79 | 1,95 | 0.92 | |
9 | 124,25 | RF | 1,20 | 1,39 | 0.86 | |
10 | RH_06 | 25,75 | KO | 1,40 | 1,61 | 0.87 |
11 | 38,00 | PF | 1,45 | 1,61 | 0.90 | |
12 | 107,00 | RF | 1,25 | 1,79 | 0.70 | |
2011 | ||||||
1 | BA_01 | 88,25 | KO | 2,20 | 2,40 | 0.92 |
2 | 27,50 | PF | 2,27 | 2,48 | 0.91 | |
3 | 225,25 | PF2 | 1,65 | 1,79 | 0.92 | |
4 | 187,75 | RF | 1,18 | 1,39 | 0.85 | |
5 | BA_02 | 25,00 | KO | 1,84 | 2,20 | 0.84 |
6 | 185,75 | PF | 1,46 | 1,61 | 0.91 | |
7 | 305,25 | RF | 1,51 | 1,61 | 0.94 | |
8 | MO_03 | 19,50 | KO | 2,03 | 2,30 | 0.88 |
9 | 29,00 | PF | 2,12 | 2,30 | 0.92 | |
10 | 211,50 | PF2 | 0,95 | 1,10 | 0.86 | |
11 | 276,00 | RF | 1,56 | 1,79 | 0.87 | |
12 | MO_06 | 22,50 | KO | 1,84 | 2,08 | 0.88 |
13 | 227,50 | PF | 1,65 | 1,79 | 0.92 | |
14 | 93,50 | RF | 1,35 | 1,61 | 0.84 | |
Die für die verschiedenen Beprobungsflächen berechneten Diversitätsindizes H bestätigen die bereits in den Abbildungen zum relativen Anteil der einzelnen Arten an der Gesamtabundanz erkennbaren Auswirkungen steigender Kupfergehalte im Boden auf das Auftreten insbesondere endogäischer Arten. Die Abb. 12 zeigt die negative Beziehung zwischen Kupfergehalt und dem Diversitätsindex H.
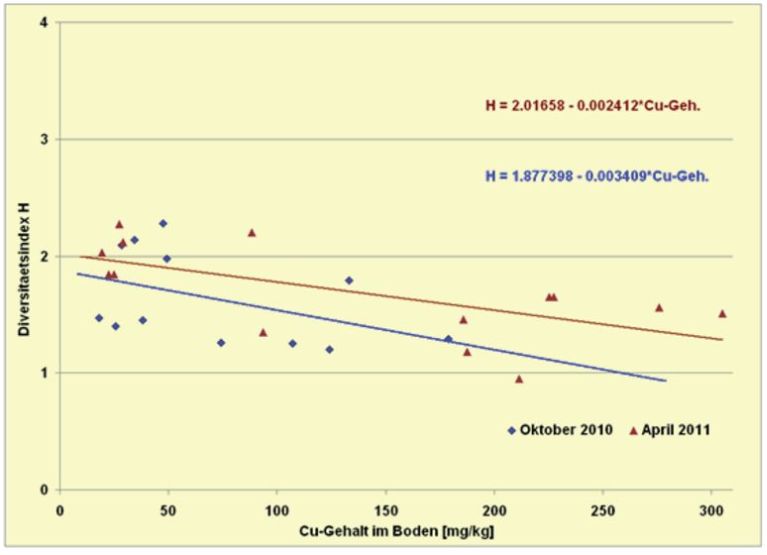
Abb. 12. Beziehung zwischen den Kupfergesamtgehalten der beprobten Flächen von je 2 Betrieben in der Pfalz, Rheinhessen, Baden und an der Mosel und den jeweiligen Diversitätsindizes (H) im jeweiligen Beprobungszeitraum.
Mittelwertvergleich der Gesamtabundanzen und der Abundanzen je Lebensformtyp mit Hilfe der Prozedur GLM und des multiplen Range-Test nach Ryan-Einot-Gabriel-Welsch der SAS®-Version 9.3. (s. Tab. 5.)
Tab. 5. Signifikant geringere Abundanzen in den Versuchsgliedern Prüffläche (PF) und Referenzfläche (RF) im Vergleich mit der Kontrolle (** signifikant bei p ≤ 0.05. nicht signifikant: n.s.). Kupfergesamtgehalte > 100 < 200 hellgrau unterlegt. Kupfergesamtgehalte > 200 dunkelgrau unterlegt
Betrieb | Prüfglied | [mg/kg Boden TM] | signifikanter Unterschied zur Kontrolle (p ≤ 0.05) | |||
Abundanz [Ind./m2] | ||||||
gesamt | anez. | endog. | epig. | |||
PF_02 | PF | 74 | n.s | n.s | n.s | – |
RF | 49 | n.s | n.s | n.s | n.s. | |
PF_03 | PF | 179 | n.s | ** | ** | – |
RF | 34 | n.s | n.s. | n.s. | n.s. | |
RH_04 | PF | 133 | n.s. | ** | n.s. | – |
RF | 124 | ** | n.s. | ** | – | |
RH_06 | PF | 38 | n.s | n.s. | n.s. | – |
RF | 107 | n.s | n.s. | n.s. | – | |
BA_01 | PF2 | 225 | n.s | n.s. | n.s. | n.s. |
RF | 188 | n.s | ** | n.s. | n.s. | |
BA_02 | PF | 186 | ** | ** | ** | – |
RF | 305 | ** | ** | ** | n.s. | |
MO_03 | PF2 | 212 | ** | – | ** | n.s. |
RF | 276 | ** | – | – | n.s. | |
MO_06 | PF | 227 | n.s | n.s | ** | n.s |
RF | 93 | n.s | n.s | ** | n.s | |
∑ f ** | 5 | 5 | 7 | 0 | ||
Schlussfolgerung: Signifikante Unterschiede zwischen den Abundanzen der Prüf- und Referenzflächen einerseits und den Kontrollflächen andererseits finden sich mit einer Ausnahme nur bei Flächen mit Gesamtgehalten > 100 mg Cu/kg Boden TM und am häufigsten beim Lebensformtyp der endogäischen Arten.
Anwendung der kanonischen Diskriminanzanalyse. Die kanonischen Diskriminanzanalyse (CANDISC, SAS®) wird hier als multivariates Verfahren zur Untersuchung des Standorteinflusses auf die Abundanzausprägung angewandt. Neben der Einflussgröße Kupfergehalt im Boden können bei einem Freilandmonitoring eine Vielzahl weiterer Faktoren auf den gewählten Endpunkt (Abundanz, Biomasse, Artenzahl) Einfluss nehmen. Da anders als im Laborversuch viele dieser Einflussgrößen nicht beherrschbar sind, bleibt die Frage offen, welche Einflüsse neben dem zu untersuchenden Hauptfaktor eine bedeutende Rolle spielen oder gar von größerer Bedeutung sind. Bei solchen Fragestellungen können multivariate Verfahren wie die kanonische Diskriminanzanalyse zur Anwendung kommen.
Folgende Fragestellungen sollten beantwortet werden:
• Welche Standortparameter führen zu unterschiedlichen Abundanzklassen? |
• Ist es tatsächlich der Kupfergehalt oder sind es eher bestimmte Bodeneigenschaften? |
Als erster Schritt wird bei der Diskriminanzanalyse eine Gruppierung über eine (nominale) Gruppierungsvariable vorgegeben. Im zweiten Schritt werden je nach Zahl und Streuung der „erklärenden“ Merkmale Diskriminanzvariablen (kanonischen Variablen) der Elemente errechnet.
Aus den folgenden Festlegungen ergeben sich die in Tab. 6 angegebenen Klassengrößen und Freiheitsgrade:
• Gruppierungsvariable: Abundanzklassen
| ||||||||||||||||||||
• Merkmalskombinationen: Cu-Gesamtgehalt, pH, Sand, Ton, org. Substanz, N |
• Gliederung nach Lebensformtypen: AN, EN und EP |
Die kanonische Diskriminanzanalyse dient der Ableitung kanonischer Variablen, die bei einer gegebenen Klassifikationsvariablen (hier: Abundanzklassen) und verschiedenen quantitativen Variablen (hier: Cu-Bodengehalt, Bodenparameter) die Zwischenklassen-Streuungen aufsummieren.
Ergebnisse der kanonischen Diskriminanzanalyse. (s. Tab. 7, Tab. 8, Tab. 9)
Tab. 7. Eigenwerte der beiden Diskriminanzvariablen (kanonischen Variablen). Eigenwerte beschreiben das maximale Verhältnis der Varianz zwischen und innerhalb der Gruppen
Lebensform | Eigenwert | Differenz | Proportion | Kumulativ | |
anezisch (AN) | 1 | 0,32 | 0,26 | 0,85 | 0,85 |
2 | 0,06 | 0,15 | 1,00 | ||
endogäisch (EN) | 1 | 0,75 | 0,69 | 0,93 | 0,93 |
2 | 0,06 | 0,07 | 1,00 | ||
epigäisch (EP) | 1 | 0,93 | 0,86 | 0,93 | 0,99 |
2 | 0,07 | 0,07 | 1,00 |
Tab. 8. Test von H0. Die kanonischen Korrelationen der jeweiligen Diskriminanzvariablen mit der Klassifizierungvariablen (Abundanzklassen) sind null. Eine Ablehnung der Nullhypothese weist auf für die Klassifizierungsvariable relevante Varianzanteile
Lebensform | Likelihood- | Approx. | Zähler | Nenner | Pr > F | |
anezisch (AN) | 1 | 0,72 | 1,62 | 14 | 126 | 0,08 |
2 | 0,95 | 0,61 | 6 | 64 | 0,72 | |
endogäisch (EN) | 1 | 0,54 | 3,27 | 14 | 126 | 0,00 |
2 | 0,94 | 0,64 | 6 | 6 | 0,70 | |
epigäisch (EP) | 1 | 0,49 | 3,91 | 14 | 126 | 0,00 |
2 | 0,94 | 0,74 | 6 | 64 | 0,62 |
Tab. 9. Standardisierte kanonische Koeffizienten zur Beschreibung der relativen Bedeutung einzelner Merkmalsvariablen für die Gruppenzuordnung bei den unterschiedlichen Lebensformen
Lebensform | Variable | Can1 | Can2 |
anezisch (AN) | Cu-Konz. | 0,11 | –0,25 |
pH | 0,91 | 0,24 | |
Sand | 0,17 | 1,02 | |
Ton | 0,86 | 0,10 | |
org. S. | –2,12 | –1,56 | |
org. C. | 1,49 | 1,70 | |
N | 0,38 | 0,22 | |
endogäisch (EN) | Cu-Konz. | 1,23 | 0,15 |
pH | 0,04 | 1,55 | |
Sand | –0,56 | 0,39 | |
Ton | –0,51 | –0,14 | |
org. S. | –0,06 | –1,09 | |
org. C. | –0,01 | 0,51 | |
N | 0,36 | 0,22 | |
epigäisch (EP) | Cu-Konz. | –0,10 | 0,41 |
pH | –0,04 | –0,39 | |
Sand | 1,37 | –1,15 | |
Ton | –0,20 | –0,39 | |
org. S. | 0,04 | –1,17 | |
org. C. | 0,38 | 1,33 | |
N | –0,02 | 0,88 |
Anezisch lebende Arten (AN): Die univariaten Teststatistiken ergaben signifikante Unterschiede zwischen den Klassen nur bei den Variablen pH und Sand-/Tonanteil. Die multivariaten Teststatistiken wiesen auf eine schlechte Trennkraft der Diskriminanzfunktion hin (Wilk‘s Lambda: 0,72 mit Pr > F 0,0828)
Korrelation der kanonischen Variablen can 1 und can 2 mit der Klassenvariablen (Abundanzklassen):
can 1: R2 = 0,24
can 2: R2 = 0,05
Die hier angegeben Ergebnisse der kanonischen Diskriminanzanalyse zeigen, dass der Hauptanteil der Varianz
zwischen den Gruppen sich bei den anezischen Arten aus Bodeneigenschaften und nicht aus dem Kupfergehalt (Konz) erklären lässt.
Endogäisch lebende Arten (EN): Die univariaten Teststatistiken ergaben signifikante Unterschiede zwischen den Klassen bei den Variablen Cu-Gehalt, pH und N. Die multivariaten Teststatistiken wiesen auf eine gute Trennkraft der Diskriminanzfunktion hin (Wilk‘s Lambda: 0,648 mit Pr > F 0,0002)
Korrelation der kanonischen Variablen can 1 und can 2 mit der Klassenvariablen (Abundanzklassen):
can 1: R2 = 0,43
can 2: R2 = 0,06
Die hier angegeben Ergebnisse der kanonischen Diskriminanzanalyse zeigen, dass der Hauptanteil der Varianz zwischen den Gruppen sich bei den endogäisch lebenden Arten aus dem Kupfergehalt im Boden und der Bodentextur sowie N-Gehalt erklären lässt.
Epigäisch lebende Arten (EP): Die univariaten Teststatistiken ergaben signifikante Unterschiede zwischen den Klassen bei den Variablen Cu-Gehalt, pH und N. Die multivariaten Teststatistiken wiesen auf eine gute Trennkraft der Diskriminanzfunktion hin (Wilk‘s Lambda: 0,485 mit Pr > F 0,0001)
Korrelation der kanonischen Variablen can 1 und can 2 mit der Klassenvariablen (Abundanzklassen):
can 1: R2 = 0,48
can 2: R2 = 0,06
Die hier angegeben Ergebnisse der kanonischen Diskriminanzanalyse zeigen, dass der Hauptanteil der Varianz zwischen den Gruppen sich bei den endogäisch lebenden Arten aus der Bodentextur und dem Corg-Gehalt erklären lässt.
Zusammenfassung der Ergebnisse der Diskriminanzanalyse: Kupfer als maßgebliche Einflussgröße spielt hiernach nur bei den endogäischen Arten eine entscheidende Rolle bei der Zuordnung zu einer der Abundanzklassen. Bei den anderen zwei Lebensformtypen sind es eher Bodenparameter wie die Textur oder die Nährstoffversorgung (Tab. 10).
Tab. 10. Merkmalskombinationen zur Erklärung der Streuung zwischen den Abundanzklassen. gegliedert nach Lebensformtypen der 2010 und 2011 beprobten Regenwurmzönosen. Der Schattierungsgrad steht für die Bedeutung des Merkmals für die Zugehörigkeit zur Gruppenvariablen (Abundanzklassen)
Lebensform | Varianzanteil der Merkmalsvariablen | ||||||
Cu | pH | Sand | Ton | org. S | org. C | N | |
AN | |||||||
EN | |||||||
EP | |||||||
Aufnahme- und Anreicherungsverhalten gemessen an extrahierten Würmern. Zur Darstellung des Aufnahmeverhaltens der Regenwürmer und zur Interpretation der beobachteten Effekte wurden von extrahierten Würmern, die zur taxonomischen Bestimmung ins Labor versandt wurden, Individuen zur Bestimmung des Kupfergehaltes entnommen und nach Vorbehandlung gemäß OECD Richtlinie 217 (OECD, 2010) unter Verwendung des Druckaufschlussverfahrens (UBA Texte, 1995a) auf ihren Gehalt an Kupfer im Wurmgewebe untersucht. Die mittleren Kupfergehalte, die in den beiden Beprobungsjahren in extrahierten Würmern gemessenen wurden, sind in Abb. 13a und 13b dargestellt. Unter der Annahme, dass unter Freilandbedingungen bei der Aufnahme von Kupfer durch den Wurm ein „steady state“ erreicht ist, wurde der Anreicherungsfaktor AF durch das Verhältnis aus der Konzentration im Wurm Kw [mg/kg Frischmasse] und der Bodenkonzentration Kb [mg/kg Trockenmasse] gebildet. Das Verhältnis von Wurmfrischmasse zu Trockenmasse beträgt nach Untersuchungen von Vespermann et al. (2003) für eine Mischprobe aus 70% endogäischen und 20% epigäischen und 10% anezischen Arten 0,25. Zu Vergleichszwecken lassen sich die auf Frischmasse bezogenen internen Cu-Gehalte durch Multiplikation mit dem Faktor 4 auf die Bezugsgröße Trockenmasse umrechnen.
![Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern des Beprobungsjahres 2010.](bilder/riepert_et_al_bld-013a.jpg)
Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern des Beprobungsjahres 2010.
![Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern des Beprobungsjahres 2011.](bilder/riepert_et_al_bld-013b.jpg)
Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern des Beprobungsjahres 2011.
Beide Abbildungen zeigen, dass die gemessenen mittleren Kupfergehalte der auf den Flächen mit höherer Kupferbelastung, wie den Prüf- oder Referenzflächen, extrahierten Würmer deutlich höhere Gehalte aufweisen, als jene der Kontrollflächen. Bei 2 Betrieben, BA_01 und BA_02, wo 2 Prüfflächen mit deutlichen Unterschieden in den Cu-Gehalten der Böden in die Beprobung einbezogen wurden, sind die Cu-Gehalte der Würmer von Flächen mit den geringen Gehalten (s. Tab. 3) denen der Kontrolle ähnlich.
Dass die Aufnahme von Kupfer aus dem Lebensraum der Würmer auch von der Lebensform abhängig ist, zeigt Abb. 13c, wo flächenunabhängig, d.h. unabhängig vom Gruppierungsmerkmal „Prüfglied“, die relativ geringe Aufnahme durch endogäisch lebende Würmer erkennbar wird. Eine deutlich höhere Kupferaufnahme weisen die Tiefengräber auf, die anders als die Mineralbodenbewohner nicht geophag sind, sondern sich saprophag ernähren und aus dem Auflagehorizont leben. Da zu wenig endogäische Würmer der beiden hoch belasteten Prüfflächen (PF2) der Betriebe BA_01 (225 mg Cu/kg Boden TM) und MO_03 (211 mg Cu/kg Boden TM) lebend im Labor angekommen sind, wurde in Abb. 14ac für das Prüfglied PF_2 der Messwert für diese Lebensform nicht berücksichtigt.
![Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern aller Beprobungen (2010 + 2011) der 3 Lebensformtypen, anezische Arten (AN), endogäische Arten (EN) und epigäische Arten (EP) gruppiert nach Prüfgliedern Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF).](bilder/riepert_et_al_bld-013c.jpg)
Abb. 13. Mittlere Kupfergehalte [mg Cu/kg Wurmfrischmasse] in extrahierten Würmern aller Beprobungen (2010 + 2011) der 3 Lebensformtypen, anezische Arten (AN), endogäische Arten (EN) und epigäische Arten (EP) gruppiert nach Prüfgliedern Kontrolle (KO), Prüfflächen (PF/PF2) und Referenzfläche (RF).
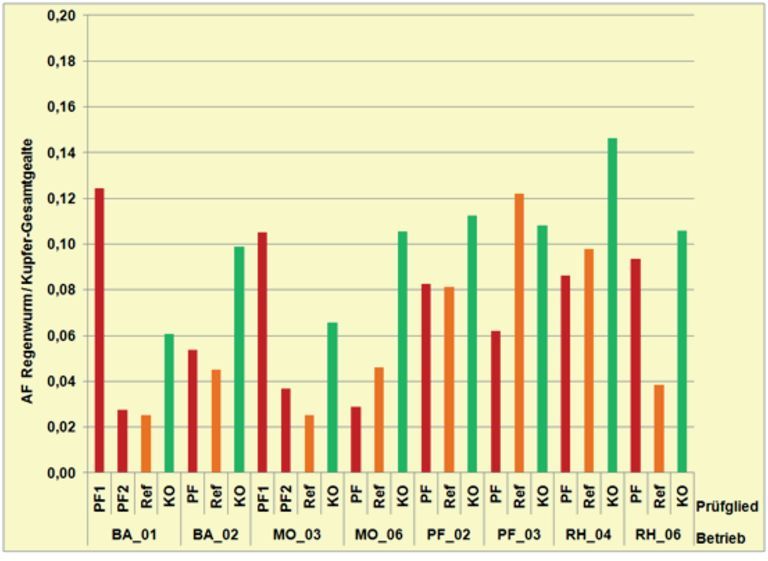
Abb. 14. Anreicherungsfaktoren (AF = Kw/Kb) bezogen auf Gesamtkupfergehalte im Boden beprobter Prüfglieder gruppiert nach Betrieben.
Ein etwas anderes Bild als bei der Betrachtung der Cu-Konzentrationen im Wurm ergibt sich für die Anreicherungsfaktoren (AF = Kw/Kb), die das Verhältnis aus Konzentration im Wurm zu Konzentration im Boden abbilden. Bei Bezug auf Gesamtkupfergehalte sind die Anreicherungsfaktoren deutlich < 1, sodass von einer Anreicherung nicht gesprochen werden kann. Abgesehen davon weisen alle Prüfglieder mit geringen Gehalten, also die Kontrollflächen und auch die beiden Prüfflächen (PF) der beiden Betriebe BA_01 und MO_03 mit ähnlich niedrigen Gehalten wie die zugehörigen Kontrollflächen, stets die höchsten AF-Werte auf, was angesichts der beobachteten Effekte auf Abundanz und Dominanzstruktur der Arten eine Änderung des Aufnahmeverhaltens der Würmer vermuten lässt (Abb. 14a).
Bei Bezug auf Kupfergehalte nach CaCl2-Aufschluss (Abb. 14b), der gern als Simulationsmodell für bioverfügbare Kupfergehalte herangezogen wird, decken die Faktoren eine Spanne zwischen 5 und 45 ab und die Unterschiede zwischen den Prüfgliedern insbesondere bei den Betrieben mit geringen und mittleren Gehalten (PF_02, PF_03, RH_04 und RH_06) nivellieren sich. Generell sind unter diesen Bedingungen die AF-Werte für Würmer von Referenzflächen am niedrigsten, was für eine geringere Verfügbarkeit spricht. Die AF-Werte hoch belasteter Prüfflächen (ca. 200 mg Cu/kg Boden TM) der Betriebe BA_01, BA_02, MO_03 und MO_06 liegen mit Ausnahme des Betriebes MO_03 unterhalb der für Regenwürmer von Kontrollflächen bestimmten AF-Werte. Die Kontrollfläche dieses Betriebes war allerdings im Hinblick auf die Artendominanz stark von der endogäischen Leitart A. caliginosa geprägt (s.a. Abb. 15b), einer Art, die möglicherweise zu ausgeprägten Meidungsreaktionen oder zu einer homöostatischen Regelung der Kupferaufnahme in der Lage ist.
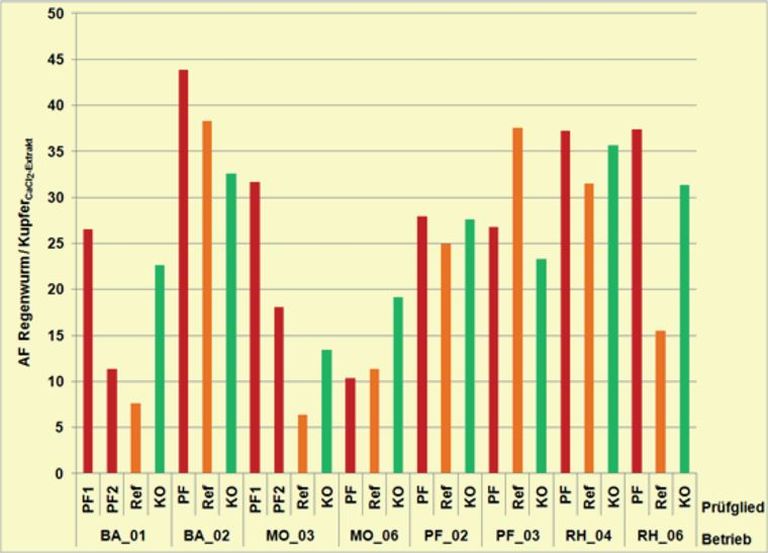
Abb. 14. Anreicherungsfaktoren (AF = Kw/Kb) bezogen auf Kupfergehalte nach CaCl2-Extraktion im Boden beprobter Prüfglieder gruppiert nach Betrieben. Die CaCl2-Extraktion von Kupfer gilt als ein Modell für die Bodenfauna verfügbarer Kupfergehalte.
![Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg TM Körper) epigäisch lebender Würmer (L. castaneum und L. rubellus) zu Cu-Gesamtgehalten [mg/kg Boden TM] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.](bilder/riepert_et_al_bld-015b.jpg)
Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg TM Körper) epigäisch lebender Würmer (L. castaneum und L. rubellus) zu Cu-Gesamtgehalten [mg/kg Boden TM] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.
Wie die Abbildungen (15a, 15b und 15c) zeigen, nehmen die internen Cu-Gehalte von Würmern der 3 Lebensformen zwar ähnlich, aber deutlich verschieden in Abhängigkeit des Beprobungszeitpunkts (Herbst im Jahr 2010 und Frühjahr im Jahr 2011) mit ansteigenden Bodengesamtgehalten zu.
![Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg TM Körper) anezisch lebender Würmer (L. terrestris und A. longa) zu Cu-Gesamtgehalten [mg/kg Boden TM] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.](bilder/riepert_et_al_bld-015a.jpg)
Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg TM Körper) anezisch lebender Würmer (L. terrestris und A. longa) zu Cu-Gesamtgehalten [mg/kg Boden TM] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.
![Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg FM Körper) endogäisch lebender Würmer (überwiegend: A. rosea, A. chlorotica und A. caliginosa) zu Cu-Gesamtgehalten [mg/kg Boden (TM)] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.](bilder/riepert_et_al_bld-015c.jpg)
Abb. 15. Gemessene interne Cu-Konzentrationen [mg/kg FM Körper) endogäisch lebender Würmer (überwiegend: A. rosea, A. chlorotica und A. caliginosa) zu Cu-Gesamtgehalten [mg/kg Boden (TM)] unterschiedlich belasteter Flächen in den Jahren 2010 und 2011 beprobter Betriebe.
Die Ergebnisse dieser Stichprobe zeigen, dass die in Würmern aller 3 Lebensformen gemessenen internen Kupferkonzentrationen mit den Bodengesamtgehalten korreliert sind (s. Tab. 11). Dabei ist der ermittelte Zusammenhang für die Herbstbeprobung 2010 für jeden Lebensformtyp deutlich enger. Dies könnte dafür sprechen, dass eine Kupferanreicherung im Gewebe von Lumbriciden im Jahresverlauf stattfindet. Bei der Frühjahrsbeprobung 2011 entfiel zunehmend die lineare Abhängigkeit von den Expositionskonzentrationen; hier wird mit einem exponentiellen Ansatz der Zusammenhang besser beschrieben. Dies könnte darauf hindeuten, dass zunächst eine hinter den Erwartungen zurückbleibende Exposition bei den langjährig bewirtschafteten Sonderkulturflächen – z.B. bedingt durch gealtertes Kupfer – vorliegt. Ferner zeigt sich auch hier, dass endogäisch lebende Arten von den Kupfergehalten im Boden am meisten betroffen sind, während die Exposition anezischer Arten weniger aus den Bodengehalten sondern aus der Nahrungsaufnahme kupferbelasteten Ernteguts zu resultieren scheint.
Tab. 11. Korrelationsanalysen für interne Cu-Konzentrationen (Kw) im Gewebe von Würmern der 3 Lebensformen und Bodengesamtgehalte (Kb) der Herbstbeprobung 2010 und der Frühjahrsbeprobung 2011 in jeweils 4 Betrieben
Beprobung | Lebensform | Regressionsgerade | r2 | P-Wert | Potentialfunktion | r2 | P-Wert |
Herbst 2010 | anezisch | Kw = 6,318 + 0,2144 * Kb | 0,79 | 0,0001 | y = 1,1724x0,6867 | 0,77 | < 0,005 |
epigäisch | Kw = 8,4916 + 0,2753 * Kb | 0,88 | 0,0008 | y = 3,36x0,4791 | 0,90 | < 0,005 | |
endogäisch | Kw = 4,1383 + 0,2734 * Kb | 0,75 | 0,0008 | y = 0,8707x07725 | 0,81 | < 0,005 | |
Frühjahr 2011 | anezisch | Kw = 10,589 + 0,1499 * Kb | 0,47 | 0,0134 | y = 1,025x0,6963 | 0,77 | < 0,005 |
epigäisch | Kw = 9,8767 + 0,0641 * Kb | 0,72 | 0,0078 | y = 2,7228x0,4016 | 0,83 | < 0,005 | |
endogäisch | Kw = 9,6314 + 0,039 * Kb | 0,15 | 0,3718 | y = 2,5163x0,3862 | 0,42 | < 0,005 |
Mit der hier beschriebenen Auswertung von Erhebungsdaten aus jeweils 3 oder in 2 Fällen auch 4 Flächen von insgesamt 8 Weinbaubetrieben wird der Versuch unternommen, einen ersten Eindruck der Auswirkungen der Anreicherung von Kupfer im Boden auf die Regenwurmzönose zu erhalten. Die Auswahl der herangezogenen Betriebe folgte einerseits Kriterien, die neben unterschiedlich hohen Kupfergehalten auch ein breites Spektrum pedologischer Größen abdecken sollte und nebenbei auch pragmatischen Gesichtspunkten wie dem Vorhandensein geeigneter Kontroll- und Referenzflächen sowie guter Zugänglichkeit folgte. Die Grundlage dafür lieferten Erhebungen zu Kupfergehalten in deutschen Qualitätsweinbaugebieten (Riepert et al., 2010 und Strumpf et al., 2011). Eine erheblich umfangreichere Beprobung im Rahmen eines öffentlich geförderten Projektes ist derzeit in Ausführung. Die während der Jahre 2010 und 2011 gesammelten praktischen Erfahrungen mit der Logistik konnten im laufenden Projekt bereits nutzbringend umgesetzt werden. Insgesamt konnten 14 Regenwurmarten identifiziert werden. Nach Dunger (1983) sind im nördlichen Mitteleuropa etwa 40 Arten nachgewiesen worden, wovon die Hälfte häufig und verbreitet ist. Insofern konnten immerhin 75% dieser häufigeren Arten während dieser Freilandstudie an Standorten in Qualitätsanbaugebieten Badens, von Rheinland-Pfalz, Rheinhessen und der Mosel gefunden werden. Die als besonders empfindlich gegenüber Kupferbelastungen geltenden endogäischen Arten Aporrectodea caliginosa, Aporrectodea rosea und besonders Allolobophora chlorotica – und deshalb auch als Indikatorarten (Belotti, 1998) vorgeschlagenen Arten – waren ausreichend vertreten. A. caliginosa und A. chlorotica gehörten zu den dominanten Arten gering belasteter Flächen.
Zur Untersuchung der Auswirkungen auf die Regenwurmzönose wurden als Endpunkte die Abundanz in ihrer Gesamtheit, gegliedert nach Standorten (Betrieben) und den untersuchten Flächen (Prüfglieder), je Lebensformtyp und nach Arten sowie die Biomasse bestimmt. Die Biomasse ist jedoch stärker als die Abundanz saisonalen Schwankungen ausgesetzt. Biomasse als Endpunkt wurde daher nur in Ergänzung der Betrachtung der Auswirkungen auf die Gesamtabundanz herangezogen.
In allen untersuchten Flächen beider Beprobungsjahre äußerten sich die Wirkungen maßgeblich in einer Reduktion der Artenzahl der endogäisch lebenden Arten (Mineralbodenbewohner). Im Falle geringerer Belastung (< 100 mg Cu/kg Boden) war diese Lebensform zwar noch zahlenmäßig präsent, aber nur durch 2 Arten, A. chlorotica und in geringem Anteil A. caliginosa vertreten. Bei hohen Gehalten (> 200 mg Cu/kg Boden TM) entfiel diese Lebensform zur Gänze und Streubewohner und Tiefengräber bestimmten die Lebensgemeinschaft bei nun auch deutlich reduzierter Gesamtabundanz. In der Mehrzahl der untersuchten Flächen aller 8 Betriebe reichte eine anteilige Auftrennung nach Lebensform aus, um Effekte auf Populationsebene sichtbar zu machen. Dieser Effekt war so deutlich, dass saisonale Unterschiede, z.B. erwähnt von Paoletti et al. (1998), wonach A. caliginosa und andere endogäische Arten im Herbst häufiger anzutreffen sind, während die anderen beiden Lebensformtypen im Verhältnis häufiger im Frühling auftreten, für die empfindlichen endogäischen Arten keine kompensierende Rolle spielte. Was die epigäischen Arten angeht, so waren bei der Herbstbeprobung stets wenig oder gar keine Vertreter dieser Lebensform in der Stichprobe, unabhängig von Gehalten und Bodenbearbeitung. Bei der Frühjahrsbeprobung wurden sie dann deutlich vermehrt angetroffen, auch in Referenzflächen mit hohen Gehalten an Kupfer. Statistische Untersuchungen unter Anwendung der kanonischen Diskriminanzanalyse mit dem Programm CANDISC (SAS 9.3) unterstützen die vorgestellten Befunde insofern, als Kupfer als Einflussfaktor für die Varianzausprägung nur bei den endogäisch lebenden Arten eine Rolle spielt. Bei den beiden anderen Lebensformen wird die Varianz vorwiegend von Faktoren wie der Bodentextur und Nährstoffversorgung bestimmt. Dieses Ergebnis entspricht den Befunden von Paoletti et al. (1998), wonach die endogäischen Arten von Kupfer stark reduziert werden, während die anezischen und epigäischen weit weniger beeinflusst werden und daher auch Weinbergpopulationen häufig von anezischen Arten dominiert werden (Cluzeau et al., 1987). Im Vergleich zu einjährigen Regenwurmfreilandtests (DIN ISO 11268-3) und ähnlichen, aber mit 10 Jahren deutlich längeren Studien wie derjenigen der EUROPEAN COPPER TASK FORCE (Klein, 2007) spiegelt eine Erhebung wie die hier beschriebene das Ergebnis einer Entwicklung wider, die sich auf der Expositionsseite zwar auch durch Alterungsprozesse auszeichnet, aber auf der Effektseite durch mannigfaltige Wirkungen, darunter auch akuten, wie insbesondere Meidungseffekten und natürlich chronischen Wirkungen auf Populationsebene gekennzeichnet ist. Geringere Bioverfügbarkeit auf Grund der Einbindung des Kupfers in stabile Verbindungen, wie sie bei klassischen längerfristigen Toxizitätstests wie dem Regenwurmreproduktionstests eine Rolle spielen kann oder ein extremes Expositionsszenario wie es durch Behandlung der Versuchsfläche, in der Regel Grünland mit hohem Regenwurmbesatz, mit kupferhaltigen Formulierung entsteht, verfälschen nicht das Bild komplexer längerfristiger Entwicklung. Über die Modellierung bioverfügbarer Kupfergehalte durch Einsatz weicherer Extraktionsverfahren wie der Kalziumchloridextraktion und die Abhängigkeit der Verfügbarkeit von Bewirtschaftungsmaßnahmen und Bodenparametern ist bereits von Strumpf und Strassemeyer (2012) berichtet worden. Der statistisch belegte Zusammenhang zwischen CaCl2-Extraktion und Gesamtgehalten nach Königswasseraufschluss wurde von den Autoren als schwach bis mittel beschrieben.
Stellt man sich die Frage, ab welchem Gesamtgehalt an Kupfer im Boden Auswirkungen sichtbar wurden, so ist zweifelsfrei erkennbar, dass bereits bei der mit 74 mg/kg vergleichsweise gering mit Kupfer belasteten Prüffläche des Betriebs PF_02 auf Artebene eine Reduktion der Arten und auch eine Dominanzverschiebung zu beobachten war. Im Vergleich zur Kontrollfläche halbierte sich der Shannon-Wiener-Index H nahezu. Ohne nun hieraus einen Schwellenwert ableiten zu können, so passt diese Beobachtung doch gut zu dem von Jänsch et al. (2007) abgeleiteten HC5-Wert von 55 mg/kg Gesamtkupfer für subletale Auswirkungen auf Bodenorganismen aus einer „Species Sensitivity Distribution (SSD)“. Darüber hinaus liegen Daten aus Meidungsversuchen an der Standardart Eisenia fetida und Freilandarten vor, die zeigen, dass bei 56 mg Cu/kg Boden TM Würmer versuchen, entsprechenden Substratkonzentrationen zu entkommen (Lukkari and Haimi, 2005). Die Ausprägung von Effekten hängt dabei zusätzlich auch von Bodenparametern wie pH-Wert, Textur und der Kationenaustauschkapazität (KAK) ab (Wightwick et al., 2008).
Die in die Beprobung einbezogenen Referenzflächen, die in aller Regel mehr als 10 Jahre nicht mehr in Nutzung standen und vom Vegetationsbild häufig einer Brache mit beginnender Sukzession glichen, insbesondere aber keiner Bodenbearbeitung mehr unterlagen, zeigten im Hinblick auf die endogäischen Arten keine Erholung der Abundanz und Artenvielfalt. In einer Untersuchung über kritische Kupfergehalte im Regenwurmkörper (Ma, 2005) wurde angemerkt, dass eine niedrige Wiederbesiedlungsrate kontaminierter Flächen bei unerwartet geringen Kupfergehalten im Körper auch einem Meidungsverhalten während der Besiedlung zuzuschreiben ist. Eijsackers et al. (2005) stellten Untersuchungen zum Grabungsverhalten der Würmer an und verglichen Weinbergsböden mit Grünland sowie Grünland mit Kupferbehandlung. Die Grabungsaktivität von A. caliginosa war in den Weinbergsböden oder dem mit dem Fungizid Kupferoxychlorid behandelten Grünland deutlich geringer, was natürlich Folgen für die Wiederbesiedelung hat. Darüber hinaus konnte insbesondere bei Böden, denen Kupfer zudotiert wurde, auch eine deutliche Wachstumsverzögerung bei den Regenwürmern beobachtet werden, die natürlich auch Auswirkungen auf die Reproduktionseffizienz hat, was ebenfalls die Wiederbesiedelung beeinträchtigt (Ma, 1982, 1988; Klok und de Roos, 1998). Unter Berücksichtigung dieses Aspektes würde eine Flächenstilllegung höher belasteter Standorte keine Verbesserung der Populationsstruktur der Regenwurmzönose erbringen.
Die internen, im Wurmgewebe bestimmten Kupfergehalte der bei der Stichprobenahme gewonnenen Würmer weisen im Hinblick auf die Standortbelastung, die untersuchten Flächen (Kontrolle, Prüf- und Referenzfläche) und die Unterteilung nach den 3 Lebensformen teilweise erhebliche Unterschiede auf. Die höchsten gemessenen mittleren Konzentrationen lagen bei 14 mg/kg Frischmasse. Auffallend ist, dass zu den beiden Beprobungsterminen im Herbst und Frühjahr die internen Cu-Gehalte bei Würmern aus den höher belasteten Prüf- und Referenzflächen signifikant gegenüber den Gehalten von Würmern aus den Kontrollen erhöht waren, sodass davon auszugehen ist, dass die Aufnahme von der Expositionskonzentration abhängig ist. Der Betrieb BA_01 stellt insofern keine Ausnahme dar, als der Gesamtgehalt der Kontrollfläche über 80 mg/kg Boden TM liegt und damit deutlich höher als der Wert der 1. Prüffläche (PF) ist. Dies führt dazu, dass der Unterschied zur Prüffläche 2 (PF2) nicht signifikant ist. Was die Aufnahmerate angeht, so ist diese vergleichbar mit Angaben aus der Literatur. Morgan und Morgan (1999) berichten bei Kupfergesamtgehalten im Boden von 62 mg Cu/kg Boden TM über interne Wurmgehalte von 20 mg Cu/kg Wurm TM bei A. caliginosa und 14 mg Cu/kg Wurm TM bei L. rubellus. Bei ähnlicher Größenordnung an Gesamtgehalten, wie sie z.B. für den Betrieb PF_02 vorliegen, finden sich durchschnittliche interne Cu-Gehalte in Würmern der Prüffläche von 6 mg/kg Frischmasse, was 24 mg/kg TM entspricht. Die Höhe der in Würmern der Frühjahrsbeprobung 2011 gemessenen internen Kupfergehalte übersteigt allerdings trotz der wesentlich höheren Kupfergehalte im Boden nicht die in Wurmproben des Beprobungsjahres 2010 gemessenen Werte, was dem Transportmechanismus von Metallen durch Zellmembranen zuzuschreiben sein könnte, der bestimmte Trägersysteme erfordert, die bei hohen externen Metallkonzentrationen nicht in ausreichendem Maß zur Verfügung stehen können (Veltman et al., 2007), und es so zu einer homöostatischen Regelung kommt. Entsprechend fallen die mittleren Anreicherungsfaktoren (AF) für Würmer aus höher belasteten Flächen auch eher gering im Vergleich gering bis mittelstark belasteten Flächen des Beprobungsjahres 2010 aus. Die gute Korrelation der internen Kupfergehalte im Regenwurmgewebe mit den Bodengesamtgehalten in der Herbstbeprobung entspricht dem, was von anderen Autoren (Veltman et al., 2007) berichtet wurde. Die Spanne der Steigungen der Regressionsgeraden zwischen 0,195 und 0,325 entspricht dem Wert von 0,27, der für Kupfer und Zink bei L. rubellus in dieser Arbeit angegeben wird. Die fehlende Korrelation für das Jahr 2011 bei den endogäischen Arten könnte angesichts der deutlich höheren Cu-Gehalte in den Prüf- und Referenzflächen an deren ausgeprägterem Meidungsverhalten liegen und auch methodisch bedingt sein, da mangels extrahierter Tiere weniger Wertepaare vorlagen. Im Gegensatz dazu können die anezischen Arten aufgrund ihrer anderen Lebensweise, die eine eher saprophage als geophage Ernährung beinhaltet weniger von der jeweiligen Höhe der Cu-Gehalte im Boden betroffen sein.
Als Ergebnis der Freilanduntersuchung hat sich herausgestellt, dass die Gesamtabundanzen (Anzahl Würmer über alle Arten) bei niedriger und mittlerer Kupferbelastung wenig aussagekräftig sind und streuungsbedingt Mittelwertvergleiche zu keinen signifikanten Unterschieden führen. Bei näherer Betrachtung der Abundanzen und Berücksichtigung der Verteilung auf die drei Lebensformen, Streubewohner (epigäisch), Mineralbodenbewohner (endogäisch) und Tiefengräber (anezisch) und erst recht bei Betrachtung der Artenzahlen, werden dagegen Auswirkungen erkennbar. In allen untersuchten Flächen äußerten sich die Wirkungen maßgeblich in einer Reduktion der Artenzahl der Mineralbodenbewohner. Im Falle geringerer Belastung (< 100 mg Cu/kg Boden TM) war diese Lebensform zwar noch zahlenmäßig präsent, aber nur durch eine Art repräsentiert. Bei hohen Gehalten (> 200 mg Cu/kg Boden TM) entfiel diese Lebensform zur Gänze und Streubewohner und Tiefengräber bestimmten die Lebensgemeinschaft bei nun auch deutlich reduzierter Gesamtabundanz. Die Abnahme des Shannon-Wiener-Index drückt diesen Sachverhalt in Zahlen aus. In der Mehrzahl der untersuchten Flächen reichte eine Auftrennung nach Lebensform aus, um Effekte sichtbar zu machen.
Die häufig beschriebene größere Empfindlichkeit geophag lebender endogäischer Arten kann nach den bisherigen Beprobungen bestätigt werden. Standortfaktoren wie Boden-pH, Korngrößenverteilung (Bodentextur) und die organische Substanz sind Faktoren die neben Bodenverunreinigungen erheblichen Einfluss auf Abundanz und Artenvorkommen nehmen können. Nur für endogäische Arten konnte Kupfer als Hauptkomponente für die Abundanzvarianz gefunden werden.
Kupfer wird mit zunehmender Expositionskonzentration vermehrt aufgenommen. Bei höheren Bodengesamtgehalten entfällt diese Korrelation und homöostatische Regelungsmechanismen greifen, weshalb die Anreicherung als solche eher gering bleibt.
Aus der Nutzung genommene Flächen wie die hier beschriebenen „Referenzflächen“ werden auch nach längerer Zeit (> 10 Jahre) nicht in der Weise wiederbesiedelt, dass die Artenvielfalt und Abundanz derjenigen naturnaher Flächen wie den Kontrollflächen entspräche.
Die in der Machbarkeitsstudie nachgewiesene Reduzierung der Artenvielfalt auf belasteten Flächen offenbart weiteren Forschungsbedarf. Welchen Beitrag leisten Singlespezies der Regenwurmzönose für eine nachhaltige Bewirtschaftung resp. den Erhalt der Bodenfruchtbarkeit auf langjährig genutzten Sonderkulturstandorten? Unter welchen Voraussetzungen ist der Wegfall einzelner Regenwurmarten bzw. von Lebensformen für die Funktionsfähigkeit der Habitate noch tolerabel?
Die Autoren danken für die Unterstützung bei den Freilanderhebungen der Regenwurmzönosen Frau Elke Reich, Frau Martina Kulcke, Christian Menzel, Tobias Hoffmann und Frau Silvia Baas. Die Autoren danken zugleich dem Labor Dr. Stefanie Krück* in Berlin für die taxonomische Bestimmung der Lumbriciden bis auf Artebene und Dr. Jörn Strassemeyer für die statistische Bewertung maßgeblicher Einflussgrößen auf die Lebensformen.
Weiterhin danken die Autoren Frau Ursula Stendel und Frau Catrin Vetter für ihre technische Assistenz bei den durchgeführten Laboruntersuchungen mit den gesammelten Regenwurm- und Qualitätsweinbaubodenproben.
Backhaus, G.F., 2011: Erfassung des Kupfergehaltes landwirtschaftlich genutzter Böden von Sonderkulturen in Deutschland – Stand, Fazit, Ausblick. Journal für Kulturpflanzen 63 (5), 129-130.
Bäumler, W., 2011: MAPPER ein Windows-Programm für Kartierungsarbeiten, Version 2.9, Deutsche Ausgabe – November 2011.
Belotti, E., 1998: Assessment of a soil quality criterion by means of field survey. Appl. Soil Ecol. 10, 51-63.
Bouché, M.B., 1977: Stratégies lombriciennes. In: Lohm, U., T. Persson (Eds.), Soil organisms as Components of Ecosystems. Stockholm, Ecological Bulletin NFR, 122-132.
Christian, E., A. Zicsi, 1999: Ein synoptischer Bestimmungsschlüssel der Regenwürmer Österreichs. Wien, Die Bodenkultur 50 (2), 121-131.
Cluzeau, D., M. Lebouvier, P. Trahen, M.B. Bouché, C. Badour, A. Perraud, 1987: Relations between earthworms and agricultural practices in the vineyards of Champagne, Preliminary results, In: Bonvicini Pagliai, A.M., P. Omodeo, (Eds.), On Earthworms. Mucchi, Modena, 465-484.
DAR, 2003: Copper, Dossier According to Directive 91/414/EEC for European Union Copper Task Force, Summary and Assessment, Document M-II (Tier II) Annex II Section 6, Point 8. Ecotoxicological studies, November 2003.
DIN, 1996: DIN ISO 10694: Katalytische Rohrverbrennung unter Sauerstoffzufuhr bei hohen Temperaturen.
DIN, 1997: DIN 19683: 2. Bodenuntersuchungsverfahren im Landwirtschaftlichen Wasserbau – Physikalische Laboruntersuchungen, Bestimmung der Korngrößenzusammensetzung nach Vorbehandlung mit Natriumpyrophosphat.
DIN, 1998: DIN ISO 13878: Katalytische Rohrverbrennung unter Sauerstoffzufuhr bei hohen Temperaturen.
DIN EN ISO 23611-1:2011-09 Bodenbeschaffenheit – Probenahme von Wirbellosen im Boden – Teil 1: Handauslese und Formalinextraktion von Regenwürmern (ISO 23611-1:2006).
Dunger, W., 1983: Tiere im Boden, Die neue Brehmbücherei. Wittenberg Lutherstadt, A. Ziemsen Verlag, 327, 280 S.
Easton, E.G., 1983: A guide to the valid names of Lumbricidae (Oligochaeta). In: Satchell, J.E. (Ed.): Earthworm Ecology – From Darwin to Vermiculture. London, New York, Chapmann and Hall, 475-487.
Felgentreu, D., F. Riepert, B. Baier, 2012: Prüfung der Auswirkungen von Pflanzenschutzmitteln auf die strukturelle Diversität in Böden. Julius-Kühn-Archiv 436, 88-93.
Graff, O., 1953: Bodenzoologische Untersuchungen mit besonderer Berücksichtigung der terrikolen Oligochaeten. Z. Plantenern. Düng. Bodenk. 106, 72-77.
Jänsch, S., J. Römbke, H.-J. Schallnass, K. Terytze, 2007: Derivation of soil values fort the path ‘soil-soil organisms’ for metals and selected organic compounds using species sensitivity distribution. Environ. Sci. Pollut. Res. 14 (5), 308-318.
Jänsch, S., J. Römbke, 2008: Einsatz von Kupfer als Pflanzenschutzmittel-Wirkstoff: Ökologische Auswirkungen der Akkumulation von Kupfer im Boden. Bericht für das Umweltbundesamt (FKZ 360 03 040), 67 S.
Klein, O., 2007: A Field Study to Evaluate the Effects of Copper on the Earthworm Fauna in Central Europe. Interim Report 2006 –Year 3. Unpublished Report Number 20031343/G1-NFEw EU COPPER TASK FORCE.
Klok, C., A.M. de Roos, 1998: Impact of toxicants on earthworm populations. A modelling approach. In: Sheppard, S., J. Bembridge, M. Holmstrup, L. Postuma (Eds.), Advances in Earthworm Ecotoxicology. ESTAC Press Pensacola, FL, S. 295-309.
Kühle, J.C., 1986: Modelluntersuchungen zur strukturellen und ökotoxikologischen Belastung von Regenwürmern in Weinbergen Mitteleuropas (Oligochaeta: Lumbricidae). Diss. Rheinische Friedrich-Wilhelms-Universität Bonn, 391 S.
Lukkari, T., J. Haimi, 2005: Avoidance of Cu- and Zn-contaminated soil by three ecologically different earthworm species. Ecotox. & Environ. Saf. 62, 35-41.
Ma, W.C., 1982: Biomonitoring of soil pollution: ecotoxicological studies of the effect of soil-borne heavy metals on lumbricid earthworms. Annual Report, Research Institute for Nature Management, Arnhem. 42-49, 83-97.
Ma, W.C., 1988: Toxicity of copper to lumbricid earthworms in sandy agricultural soils amended with Cu-enriched organic waste materials. Ecol. Bull. 39, 53-56.
Ma, W.C., 2005: Critical body residues (CBRs) for ecotoxicological soil quality assessment: copper in earthworms. Soil Biology & Biochemistry 37, 561-568.
Morgan, J.E., A.J. Morgan, 1999: The accumulation of metals (Cd, Cu, Pb, Zn and Ca) by two ecologically contrasting earthworm species (Lumbricus rubellus and Aporrectodea caliginosa): implications for ecotoxicological testing. Appl. Soil Ecol. 13, 9-20.
Neubert, E., 2012: Lumbricidenuntersuchungen auf ausgewählten Boden – Dauerbeobachtungsflächen (BDF) in Sachsen-Anhalt. Ergebnisbericht 2011. http://www.sachsen-anhalt.de/fileadmin/Elementbibliothek/Bibliothek_Politik_und_Verwaltung/Bibliothek_LAU/Umweltanalytik/Dateien/Bericht_Lumbriciden_2011.pdf; letzter Zugriff 21.06.2013.
OECD, 2010: OECD 317, OECD Guidelines For The Testing Of Chemicals, Bioaccumulation in Terrestrial Oligochaetes, 30 S.
Paoletti, M.G., D. Sommaggio, M.R. Favretto, G. Petruzzelli, B. Pezzarossa, M. Barbafieri, 1998: Earthworms as useful bioindicators of agroecosystem sustainability in orchards and vineyards with different inputs. Appl. Soil Ecol. 10, 137-150.
Riepert, F., 2009: Auswirkungen von Kupferbelastungen auf ausgewählte Indikatoren der Bodenzönose, Journal für Kulturpflanzen 61 (4), 131-139.
Riepert, F., A. Steindl, R. Eibach, M. Maixner, C. Reichmuth, J. Strassemeyer, T. Strumpf, 2010: Monitoring of total contents of copper in organically and conventionally managed soils. Part 1: Study plan and preliminary sampling of copper and other anthropogenic induced heavy metal contents in vineyard soils. Journal für Kulturpflanzen 62 (2), 42-50.
Riepert, F., D. Felgentreu, T. Strumpf, 2012a: Auswirkungen von Kupfereinträgen im Weinbau auf die Regenwurmzönose – Ergebnisse von Labortests und Feldbeprobungen. VDLUFA Schriftenreihe 68/2012 147-157.
Riepert, F., B. Baier, D. Felgentreu, T. Strumpf, 2012b: Regenwurmzönosen als Indikatoren der Bodenfruchtbarkeit am Beispiel weinbaulich genutzter Flächen. Julius-Kühn-Archiv 436, 37-43.
Scott-Fordsmand, J.J., J.M. Weeks, S.P. Hopkins, 2000: Importance of contamination history for understanding toxicity of Copper to earthworm Eisenia fetida (Oligochaeta: Annelida), using neutral-red retention assay. Environ. Toxicol. & Chem. 19 (7), 1774-1780.
Sims, R.W., B.M. Gerard, 1999: Earthworms: Notes for the identification of British Species. 4th Edition. Published for The Linnean Society of London and The Estuarine and Coastal Sciences Association by Field Studies Council, Montford Bridge, Shrewsbury, UK, pp 1-169.
Spellerberg, I.F., P.F. Fedor, 2003: A tribute to Claude Shannon (1916–2001) and a plea for more rigorous use of species richness, species diversity and the ‘Shannon-Wiener’ Index. Global Ecology & Biogeography 12, 177-179.
Strumpf, T., F. Riepert, D. Felgentreu, 2012a: Kupfermonitoring in Deutschland (Aktueller Stand, Ergebnisse und Ausblick) in Fachgespräch: „Kupfer als Pflanzenschutzmittel“, Berichte aus dem Julius Kühn-Institut 164, 6-7.
Strumpf, T., A. Steindl, J. Strassemeyer, F. Riepert, 2011: Erhebung von Kupfergesamtgehalten in ökologisch und konventionell bewirtschafteten Böden. Teil 1: Gesamtgehalte in Weinbergsböden deutscher Qualitätsanbaugebiete. Journal für Kulturpflanzen 63 (5), 131-143.
Strumpf, T., F. Riepert, D. Felgentreu, 2012b: Erhebung von Gesamtkupfer, anderen anthropogen eingetragenen Schwermetallen und Nährelementen in ökologisch und konventionell bewirtschafteten Böden deutscher Wein-, Hopfen- und Baumobstgebiete – ein Statusbericht. VDLUFA Schriftenreihe 68/2012, 137-147.
Strumpf, T., J. Strassemeyer, 2012: Bioverfügbare Kupfergehalte in ökologisch und konventionell bewirtschafteten Böden deutscher Wein-, Hopfen- und Baumobstgebiete. Teil 5: – Bestimmung des bioverfügbaren Anteils von Kupfer und anderen Schwermetallen durch CaCl2-Extraktion. Journal für Kulturpflanzen 64 (12), 452-468.
UBA Texte, 1995: Methodenhandbuch Bodenschutz Teil 1, 10/95, Druckaufschluss mit HF/HCLO4/HNO3; ISSN 0722-186X, S. 49.
VDLUFA, 1991a: Methodenbuch, Band I. Die Untersuchung von Böden, A 2.4.3.1. VDLUFA-Verlag Darmstadt; DIN, 1983: DIN 38414, Teil 7. Aufschluss mit Königswasser zur nachfolgenden Bestimmung des säurelöslichen Anteils von Metallen. Berlin, Beuth Verlag.
VDLUFA, 1991b: Methodenbuch, Band I. Die Untersuchung von Böden, A 5.1.1. Darmstadt, VDLUFA-Verlag.
Veltman, K., M.A.J. Huijbregts, M.G. Vijver, W.J.G.M. Peijnenburg, P.H.F. Hobbelen, J.E. Koolhaas, C.A.M. Van Gestel, P.C.J. Van Vliet, A.J. Hendriks, 2007: Metal accumulation in the earthworm Lumbricus rubellus. Model predictions compared to field data. Environmental Pollution 146, 428-436.
Vespermann, A., F. Riepert, J. Pflugmacher, 2003: Untersuchungen zur Aufnahme von HCB und Pyren durch den Kompostwurm Eisenia fetida und ausgewählte Regenwurmwildarten – Ableitung eines Bioakkumulationstests. UWSF – Z. Umweltchem. Ökotox. 15 (3), 143-151.
Wightwick, A.M., M.R. Mollah, D.L. Partington, G. Allinson, 2008: Copper Fungicide Residues in Australian Vineyard Soils. J. Agric. Food Chem. 56, 2457-2464.
Fußnoten:
Freie Beraterin Pflanzenbauliche Forschung, Bodenbiologie, Warthe Str. 13, 12051 Berlin |