

Einfluss von Kupfer auf die Aktivität von Bodenmikroorganismen in ausgewählten Böden deutscher Weinanbaugebiete
Influence of copper on the activity of soil microorganisms in selected German vineyards
Journal für Kulturpflanzen, 65 (12). S. 466–478, 2013, ISSN 1867-0911, DOI: 10.5073/JfK.2013.12.02, Verlag Eugen Ulmer KG, Stuttgart
Seit 2009 wurden Kupfer-Gesamtgehalte auf unterschiedlich bewirtschafteten Flächen deutscher Qualitätsweinbaubetriebe bestimmt. Nach Auswahl von geeigneten Flächen mit großer Breite an Cu-Gesamtgehalten, Bodeneigenschaften und Bewirtschaftungsformen erfolgt eine Abschätzung möglicher Auswirkungen auf Regenwurmzönosen und Bodenmikroorganismen. In einer Machbarkeitsstudie erfolgte eine biologische Zustandserhebung auf Flächen von acht Qualitätsweinbaubetrieben aus den Anbaugebieten Rheinland-Pfalz, Rheinhessen, Baden und Mosel auf Parameter der Gemeinschaften von Bodenmikroorganismen, die im Herbst 2010 und Frühjahr 2011 beprobt wurden.
Bei allen untersuchten Böden wurden nur die in den Böden vorhandenen autochthonen Populationen geprüft. Diese Populationen waren höheren Cu-Gehalten mehr als 50 Jahre ausgesetzt, so dass eine Anpassung der Mikroorganismen an die natürlichen Standortbedingungen über die Ausbildung von Kupferresistenzen und Toleranzen erfolgt sein könnte.
Die Ergebnisse der Untersuchung der Bodenatmung, Dehydrogenaseaktivität und potentiellen Nitrifizierung sowie weiterer bestimmter Parameter wie mikrobielle Biomasse, metabolischer Quotient und Cmik/Corg-Verhältnis werden in Zusammenhang mit bioverfügbaren und Gesamtgehalten an Kupfer und physiko-chemischen Bodeneigenschaften diskutiert. Dabei wurden die Prüfflächen mit den zugeordneten unbehandelten Kontrollflächen verglichen.
Ein enger Zusammenhang zwischen steigendem Kupfergehalt und nachhaltiger Beeinflussung der Aktivität der Mikroorganismen in den untersuchten Böden konnte jedoch nicht gefunden werden. Andere Bodenparameter scheinen die Aktivitäten deutlicher zu beeinflussen.
Dies könnte daran liegen, dass die Bioverfügbarkeit von Kupfer multifaktoriell beeinflusst wird (z.B. Korngrößenverteilung, organischer Kohlenstoffgehalt, Kationenaustauschkapazität, pH-Wert) und zusätzlich Prozesse der Alterung und Sequestrierung die Toxizität gegenüber bodenbürtigen Mikroorganismen zu reduzieren scheinen.
Stichwörter: Weinbau, Bodenbelastung, Kupfergesamtgehalte, Auswirkungen auf Mikroorganismen im Boden, Aktivitäts- und Summenparameter
Since 2009, total copper contents were determined on different main wine culturing regions of Germany. After the selection of suitable areas which differed in the total Cu concentrations, soil properties and farming systems, an estimation of possible effects on earthworm communities and soil microorganisms was carried out. In a feasibility study a biological condition survey was performed to eight areas of quality wine producers from the vineyards of Rheinland-Pfalz, Rheinhessen, Baden and Moselle on the parameters of soil microbial communities that were sampled in autumn 2010 and spring 2011.
In all investigated soils only the soil autochthonous populations were examined. These populations were exposed to higher Cu contents for more than 50 years, and thus the microorganisms adapted to the natural site conditions on the formation of copper resistance and tolerance.
The results of the investigation of soil respiration, activity of dehydrogenase and potential nitrification, and other specific parameters such as microbial biomass metabolic quotient, and Cmic/Corg ratio are discussed in the context of bioavailable and total contents of copper and physico-chemical soil properties. The test soils were compared with the corresponding untreated control.
However, a strong correlation between increasing copper content and lasting influence on the activity of the microorganisms in the studied soils could not be found. Other soil parameters seem to better influence such activities.
This could be related to the fact that the bioavailability of copper is influenced by other parameters (for example, particle size distribution of organic carbon, cation exchange capacity, pH). In addition, aging and sequestration processes can reduce the toxicity against soil-borne microorganisms.
Key words: Viticulture, soil pollution, total copper concentrations, effects on soil microorganisms, activity and sum parameters
Mikroorganismen spielen für eine nachhaltige Bodenfruchtbarkeit eine bedeutende Rolle. Sie sind am Ab- und Umbau der vorrangig pflanzlichen organischen Substanz beteiligt und tragen so zum Nährstoffkreislauf bei. Die physiko-chemischen Eigenschaften des Bodens, Mikroklima und Pflanzenbewuchs bestimmen hauptsächlich Abundanz und Diversität der mikrobiellen Gemeinschaft an einem Standort. Aufgrund der Heterogenität des Bodens ist auch das Vorhandensein der Mikroorganismen an sehr kleinräumige Strukturen angepasst. Neben aeroben Bereichen im Porensystem des Bodens kommen anaerobe und fakultativ anaerobe Bereiche vor. Bakterien benötigen zur Verbreitung im Boden wasserführende Schichten. Bei längerer Trockenheit kann es zum völligen Erliegen der mikrobiellen Aktivität kommen. Der Einsatz von z.B. bodenwendenden Techniken kann das Habitat der autochthonen Mikroorganismen extrem verändern, so dass es kurzfristig zum Absterben von über 95% der vorhandenen Mikroflora kommt. Auch der Eintrag von anthropogenen Stoffen kann zu Störungen und zu Hemmungen der mikrobiell getragenen Funktionen für eine nachhaltige Bodenfruchtbarkeit führen (Kandeler et al., 1996; Van-Zwieten et al., 2004). Bei Pflanzenschutzmitteln werden z.B. bewusst Wirkstoffe eingesetzt, die im Idealfall nur die Schadorganismen gezielt angreifen. Zum gegenwärtigen Zeitpunkt gibt es kein Mittel, das diese umweltschonende Selektivität besitzt.
Im Gegensatz zu organischen Pflanzenschutzmitteln wird Kupfer im Boden nicht abgebaut. Bei wiederholter und langjähriger Anwendung kommt es zur Anreicherung und kann schädigend auf viele Bodenorganismen wirken (Oliveira und Pampulha, 2006).
Kupfer ist aber auch ein essentielles Element für alle lebenden Organismen. Mikroorganismen benötigen eine konstant geringe Versorgung. Es spielt eine große Rolle in den Prozessen der Energiegewinnung, bei der Atmung und Photosynthese und ist Cofaktor für eine Reihe von Enzymen wie Superoxiddismutase, Cytochrom-c-oxidase oder Nitritreduktasen (Clemens, 2001). Alle Böden enthalten natürlich vorkommendes Kupfer. Der durchschnittliche Cu-Gehalt der kontinentalen Erdkruste beträgt 35 mg/kg, in Gesteinen 4 bis 90 mg/kg (Scheffer und Schachtschabel, 1982). In die Luft gelangt das Element mehrheitlich durch die Verbrennung von fossilen Brennstoffen und von Wind getragenem Staub. Erzabbau und die Produktion von Phosphatdüngern führt zu erhöhten Gehalten in der Nähe von Minen (Covelo et al., 2008), Fabriken und Deponien. Die Cu-Gehalte in anthropogen nicht belasteten Ackerböden betragen zwischen 8 bis 42 mg Cu/kg (Kratz et al., 2009).
In der Bundes-Bodenschutz- und Altlastenverordnung (BBodSchV, 1999) wurden im Sinne eines vorbeugenden Schutzes der Ressource Boden strenge Vorsorgewerte für Kupfer-Gesamtgehalte von 20 mg für sandige und 60 mg Cu/kg Boden TM für tonhaltige Böden festgelegt. Dies erfolgte deshalb, weil eine Beschränkung auf bloße Gefahrenabwehr zu einer Vernachlässigung von Beeinträchtigungen führen würde, die zwar die Gefahrenschwelle nicht überschreiten, in ihrer Dimension jedoch längerfristig Gefahren hervorrufen können und daher bereits jetzt ein Besorgnispotential darstellen.
Die Gesamtgehalte von Kupfer schwanken im Boden stark. Böden mit sehr niedrigen und sehr hohen Gehalten an organische Substanz sowie Kalkböden enthalten meist sehr wenig Kupfer. Die Verfügbarkeit für Pflanzen wird vor allem vom pH-Wert des Bodens (Steindl et al., 2011), dem Gehalt an organischer Substanz und der Bindungsart (z.B. Bildung stabiler organischer Komplexe; der Sorption an Oxide und Tonminerale und der Festlegung als Carbonate, Hydroxide und Phosphate) bestimmt (Giller et al., 2009; Tao et al., 2003; Bertrand et al., 2002).
Allerdings ist der Gesamtgehalt (Königswasseraufschluss) von Metallen im Boden ein schlechter Indikator für die aktuelle Konzentration in der Bodenlösung (Yu et al., 2002), die einen Effekt auf die Bodenmikroorganismen haben kann.
In den letzten Jahren sind die Anwendungen und Aufwandmengen an kupferhaltigen Pflanzenschutzmitteln (PSM) insbesondere im Ökologischen Landbau stark zurückgegangen, wie in einem Statusbericht der Anbauverbände (Wilbois et al., 2009) berichtet wurde.
Aufgabe der Untersuchungen war es, in einer Stichprobe zu überprüfen, ob die langjährige Anwendung von Kupfer im Weinbau zu einer Beeinflussung der für die Bodenfruchtbarkeit bedeutsamen Bodenmikroorganismen, insbesondere bei höheren Cu-Gesamtgehalten, führt.
Die Ergebnisse der Untersuchung der Bodenatmung, Dehydrogenaseaktivität und schneller Ammoniumoxidation sowie weiterer bestimmter Parameter wie mikrobielle Biomasse, metabolischer Quotient und Cmik/Corg-Verhältnis wurden in Zusammenhang mit bioverfügbaren und Gesamtgehalten an Kupfer und physiko-chemische Bodenparametern diskutiert. Dabei sind die Prüfflächen mit den zugeordneten unbehandelten Kontrollflächen verglichen worden.
Aus den Erfahrungen bei der Prüfung von Chemikalien (siehe ChemG, 2008) und Pflanzenschutzmitteln (PflSchG, 2012) hat sich eine Reihe von ökotoxikologischen Endpunkten bestätigt, die als biologische Indikatoren für Veränderungen und Störungen des Ökosystems Boden genutzt werden. Die in der sogenannten ökotoxikologischen Testbatterie zusammengefassten Labor-, Halbfreiland- und Freilanduntersuchungen erlauben eine biologische Charakterisierung von Böden und Bodensubstraten, die mit abiotischen Standortfaktoren verglichen werden können.
Die OECD fordert in der Richtlinie für die Prüfung von Chemikalien, Abschnitt 2: Auswirkungen auf die biotischen Systeme Labor-Untersuchungen aus dem Bereich der Kohlenstoff-Mineralisation (Test Guideline Nr. 217: Bodenmikroorganismen: Kohlenstoff-Transformations-Test) und Stickstoff-Transformation (Test Guideline Nr. 216: Bodenmikroorganismen: Stickstoff-Transformations-Test). Nationale und internationale Organisationen wie IOBC, EPPO, VDLUFA und die Normungsinstitutionen wie DIN, CEN und ISO haben dazu eine Reihe von Methoden zur Charakterisierung von Böden und Bodensubstraten beschrieben und validiert. Nach diesen Methoden erfolgte eine Bestimmung und Berechnung der Aktivitäts- und Summenparameter der Bodenmikroorganismen.
Um die Effekte einer langjährigen Anwendung von Kupfer in Weinbergsböden zu untersuchen, wurden 8 Betriebe, die über die Qualitätsweinbaugebiete Deutschlands repräsentativ verteilt sind, beprobt. Je Betrieb wurden im Regelfall 3 Versuchsglieder, eine in Bewirtschaftung befindliche Fläche (Prüffläche), eine möglichst niemals genutzte Fläche (Kontrolle) und eine ehemals genutzte Fläche (Referenz nur für Regenwurm-Tests) in die Untersuchungen einbezogen. Von jeder Fläche wurden Teile des Bodens der 4 Versuchsglieder (je 0,25 m2) im Bodenhorizont 0–20 cm entnommen, zu einer Mischprobe vereint, auf 5 mm gesiebt, in verschließbaren 15 l Polyethylen-Eimern abtransportiert und bis 1 Woche vor Versuchsbeginn im Labor bei 4°C im Dunkeln gelagert.
Bei zwei Beprobungstouren im Herbst 2010 und im Frühjahr 2011 wurden von in ökologischer oder integriert/konventioneller Bewirtschaftung befindlichen Rebflächen bekannter Historie und dazugehörigen Kontrollflächen Bodenproben für Laboruntersuchungen entnommen. Über die Beprobungsflächen und deren bodenkundliche Parameter wurde von Riepert et al. (2013, in diesem Heft, S. 440–465 – dort Tab. 2 und 3) bereits berichtet.
Tab. 2. Mikrobielle Aktivitätsparameter in ausgewählten Prüfflächen und zugeordneten Kontrollflächen
Prüfglied | Code | Extraktionsverfahren | Dehydrogenaseaktivität | Basalatmung | Subtratinduzierte Kurzzeitatmung | potentielle Nitrifikation *** | |||||||
KW | NH4NO3- | CaCl2- | |||||||||||
[mg Cu/kg TM] | [μg TPF/g TM * 16 h–1] | [mg CO2/kg TM * h–1] | [ng NO2–-N/g TM * h–1] | ||||||||||
KO | RH_04 | 18 | 0,08 | 0,13 | 8,57 | ± 0,09 | 0,91 | ± 0,1 | 7,61 | ± 0,56 | 166,47 | ± | 8,6 |
PF | 133 | 0,40 | 0,51 | 7,71 | ± 0,29** | 1,46 | ± 0,2 | 9,54 | ± 0,73 | 177,41 | ± | 10,0 | |
KO | RH_06 | 26 | 0,07 | 0,13 | 12,32 | ± 0,48 | 0,79 | ± 0,1 | 8,43 | ± 1,37 | 196,77 | ± | 8,3 |
PF | 38 | 0,56 | 0,34 | 12,21 | ± 0,12 | 0,77 | ± 0,1 | 10,48 | ± 1,05 | 136,27 | ± | 16,6 | |
KO | PF_02 | 48 | 0,11 | 0,72 | 20,39 | ± 0,69 | 2,13 | ± 0,1 | 16,10 | ± 0,42 | 415,11 | ± | 58,5 |
PF | 74 | 0,28 | 0,49 | 25,20 | ± 0,54 | 2,06 | ± 0,2 | 15,39 | ± 0,63 | 408,25 | ± | 142 | |
KO | PF_03 | 29 | 0,02 | 0,21 | 8,80 | ± 0,09 | 1,23 | ± 0,2 | 11,29 | ± 1,81 | 189,54 | ± | 4,6 |
PF | 179 | 0,46 | 0,54 | 9,09 | ± 0,29 | 1,06 | ± 0,2 | 11,67 | ± 3,24 | 205,23 | ± | 18,3 | |
KO | BA_01 | 88 | 0,25 | 0,24 | 38,48* | ± 4,47 | 1,73 | ± 0,2 | 17,73 | ± 0,34 | 417,97 | ± | 113 |
PF1 | 28 | 0,14 | 0,13 | 36,34* | ± 3,46 | 2,21 | ± 0,2 | 11,43 | ± 0,60 | 35,74 | ± | 5,2 | |
PF2 | 225 | 1,43 | 0,55 | 38,03* | ± 3,23 | 2,08 | ± 0,2 | 12,56 | ± 0,09 | 35,09 | ± | 15,4 | |
KO | BA_02 | 25 | 0,08 | 0,08 | 38,73* | ± 3,46 | 2,23 | ± 0,2 | 14,89 | ± 1,35 | 213,40 | ± | 35,3 |
PF | 186 | 0,92 | 0.23 | 47,33* | ± 2,77 | 2,51 | ± 0,1 | 14,60 | ± 1,57 | 106,96 | ± | 8,6 | |
KO | MO_03 | 20 | 0,03 | 0,29 | 43,04* | ± 1,98 | 1,99 | ± 0,3 | 18,87 | ± 0,37 | 95,08 | ± | 23,4 |
PF1 | 29 | 0,05 | 0,20 | 16,37* | ± 0,37 | 2,19 | ± 0,2 | 9,54 | ± 0,66 | 96,91 | ± | 4,6 | |
PF2 | 212 | 1,59 | 1,65 | 39,59* | ± 3,10 | 1,10 | ± 0,2 | 7,43 | ± 0,24 | 30,47 | ± | 2,4 | |
KO | MO_06 | 228 | 1,06 | 0,66 | 42,55* | ± 6,60 | 1,58 | ± 0,1 | 11,47 | ± 0,45 | 36,79 | ± | 19,6 |
PF | 228 | 1,06 | 0,66 | 42,55* | ± 6,60 | 1,58 | ± 0,1 | 11,47 | ± 0,45 | 36,79 | ± | 19,6 | |
* = Dehydrogenasaktivität bestimmt mittels INT [μg INTF/g Boden TM * 18 h–1]; **= Standardabweichung, n = 5; *** = n = 3. | |||||||||||||
Tab. 3. Berechnete mikrobielle Aktivitätsparameter in ausgewählten Prüfböden und zugeordneten Kontrollflächen
Bodentyp | Betrieb | Mikrobielle Biomasse (Cmik) | Metabolischer Quotient | Cmik/Corg-Verhältnis |
Kontrolle | RH_04 | 157,20 ± 11,5* | 5,46 ± 0,9 | 7,39 |
Prüffläche | 196,92 ± 15,1 | 4,58 ± 0,7 | 10,04 | |
Kontrolle | RH_06 | 174,13 ± 28,2 | 4,73 ± 0,6 | 5,87 |
Prüffläche | 216,27 ± 21,6 | 4,58 ± 0,8 | 5,62 | |
Kontrolle | PF_02 | 332,07 ± 8,6 | 6,96 ± 0,23 | 14,21 |
Prüffläche | 326,50 ± 13,4 | 6,47 ± 0,54 | 19,69 | |
Kontrolle | PF_03 | 232,84 ± 37,3 | 6,77 ± 0,8 | 8,94 |
Prüffläche | 240,73 ± 66,8 | 6,31 ± 1,0 | 6,14 | |
Kontrolle | BA_01 | 365,52 ± 7,1 | 4,73 ± 0,4 | 15,86 |
Prüffläche 1 | 259,14 ± 1,9 | 9,38 ± 0,8 | 10,83 | |
Prüffläche 2 | 235,77 ± 12,4 | 8,35 ± 0,6 | 10,07 | |
Kontrolle | BA_02 | 307,20 ± 27,8 | 6,82 ± 0,5 | 7,86 |
Prüffläche | 301,08 ± 32,4 | 8,40 ± 0,9 | 12,28 | |
Kontrolle | MO_03 | 179,61 ± 17,2 | 7,35 ± 0,4 | 4,35 |
Prüffläche 1 | 157,08 ± 5,7 | 6,44 ± 1,0 | 3,09 | |
Prüffläche 2 | 196,94 ± 13,6 | 10,69 ± 0,4 | 6,28 | |
Kontrolle | MO_06 | 181,72 ± 6,2 | 8,57 ± 1,3 | 3,80 |
Prüffläche | 236,56 ± 49,7 | 9,11 ± 2,9 | 7,83 | |
* = Standardabweichung; n = 5; | ||||
Diese Böden decken geringe bis mittelhohe Kupferbelastungssituationen in einem Bereich zwischen 20 mg und 350 mg Cu/kg Boden TM ab. Zwischen 2,3 und 12,5% variiert bei diesen Böden der Anteil der organischen Substanz.
Die Auswahl der Kontrollböden erfolgte auf Flächen (vergleichbare physiko-chemische Bodeneigenschaften) in geographischer Nähe, die nach Aussage der Winzer nicht in landwirtschaftlicher Nutzung waren und demzufolge eine ortstypische geogene Belastungssituation mit Kupfer widerspiegeln.
Die Lagerung der Proben im Labor erfolgte nach Bestimmung der Restfeuchte (DIN ISO 11465), pH-Wert (DIN ISO 10390) und der maximalen Wasserhaltekapazität (E DIN ISO 11274) bei 4°C in einer Kühlzelle in Dunkelheit für maximal 2 Monate.
Die Analyse der Kupfer-Gehalte erfolgte nach VDLUFA (1991). Die Bestimmung der bodenkundlichen Basisparameter wurde in Strumpf et al. (2011) beschrieben.
Die beiden Böden LAGD und K_73 (Tab. 1) sind unterschiedlich gelagerte Kontrollböden mit bekannter biologischer Charakterisierung und Verhalten im Labor.
Tab. 1. Charakterisierung der untersuchten Kontrollböden
Code | Prüfglied | Cu-Gesamt- | pH-Wert | Org. Substanz [%] | C/N Verhältnis | Bodenart | Kurzbeschreibung |
K_73 | Kontrollboden | 15 | 6,4 | 1,0 | 15,6 | Su3 | Versuchsfeld Dahlem, schluffiger Sand |
LAGD | 24 | 6,8 | 1,6 | SI2 | Langjährig vorrätig gehaltener Boden des Versuchsfeldes Dahlem |
Im Gegensatz zu den in Zucht gehaltenen faunistischen Indikatoren, die den Prüfsubstraten während der Prüfung zugesetzt werden, basieren die mikrobiologischen Prüfverfahren auf den Reaktionen der im Prüfsubstrat enthaltenen Mikroflora (autochthone Gemeinschaften). Zur Aktivierung der Populationen von Mikroorganismen wurden die Böden eine Woche vor Testbeginn auf ca. 50% der WKmax angefeuchtet und 7 Tage bei 20°C ± 1°C dunkel gelagert.
Dehydrogenasen spielen als Enzyme der Atmungskette bei der Energiegewinnung der Organismen eine wichtige Rolle. Sie sind nur für lebende Zellen sämtlicher Mikroorganismen relevant und können deshalb als Indikator für biologische Redoxsysteme und als Maß der mikrobiellen Aktivität im Boden eingesetzt werden.
Dehydrogenase-Aktivität ist ein sensitiver Indikator für eine Schwermetalltoxizität (Dick et al., 1996; Rossel et al., 1997). Die zur Bestimmung der Aktivität gemessene Formazan-Bildung kann durch das Kupfer in den Böden beeinflusst werden (Chandler und Brookes, 1991; Brookes, 1995). Deshalb wurde zur Überprüfung der Beeinflussung der Dehydrogenase-Aktivität Iodotrazoliumchlorid (INT) eingesetzt (Obbard, 2001). Eine Beeinflussung der Prüf- und Kontrollböden konnte nicht festgestellt werden.
Jeweils 5 g TS Boden werden mit 6 ml Triphenyltetrazoliumchlorid-Pufferlösung (bzw. INT-Pufferlösung) überschichtet und 16 h bzw. 18 h bei 30°C im Dunkeln inkubiert. Die Reaktion wird mit 25 ml Aceton abgestoppt. Nach weiteren 2 h wird die Lösung filtriert und spektralphotometrisch die Extinktion des gebildeten Formazans bei einer Wellenlänge von λ = 485 nm mit einem UV VIS Spektralphotometer Specord® 205 der Firma Analytik Jena AG gemessen.
Die Aktivität der Dehydrogenasen wird in μg TPF/g TM * 16 h–1 (DIN ISO 23753-1) bzw. in μg INTF/g TM * 18 h–1 (DIN ISO 23753-2) angegeben.
Die Bodenatmung, resultierend aus dem Abbau von organischen Substanzen (z.B. Mineralisierung von Ernterückständen), wird als die Sauerstoffaufnahme oder Kohlenstoffdioxidabgabe durch Bakterien, Pilze, Algen und Protozoen definiert und schließt den Gasaustausch des aeroben und anaeroben Metabolismus ein. Diese bodenbiologische Aktivität ist ein Summenparameter, wobei die CO2-Bildung die Endstufe der Kohlenstoffmineralisierung darstellt. Unter ungestörten Bedingungen stellt sich im Boden ein ökologisches Gleichgewicht ein, welches als Basal- oder Langzeitatmung (LZA) bezeichnet wird. Bei Zugabe eines leicht abbaubaren Substrates – wie Glukose – und kurzzeitiger Aktivierung der lebenden Mikroorganismen spricht man von der substratinduzierten Kurzzeitatmung (SIR).
Die Bodenproben (Wkmax ca. 50%) werden in einem geschlossenen Gefäß bei 20°C für 24 Stunden im Dunkel inkubiert und das gebildete CO2 in Natronlauge absorbiert. Der daraus resultierende Unterdruck wird manometrisch gemessen (OxiTop®-Verfahren). Die Druckänderung ist proportional zur Masse an verbrauchtem Sauerstoff. Die LZA und SIR werden in mg O2/kg Boden TM * h–1 angegeben. Mit dem Faktor 1,375 kann der Sauerstoff-Verbrauch in Kohlenstoffdioxid-Bildung umgerechnet werden [mg CO2/kg TM * h–1] (DIN EN ISO 16072).
Nach Bestimmung der optimalen Konzentration (maximale Atmungsrate bei Substratzusatz) für die jeweiligen Böden werden für die SIR-Bestimmung die Proben mit Glukose als schnell zu metabolisierendes C-Substrat versetzt und über 12 h bei 20°C im Dunkeln die unmittelbar folgende Atmungsreaktion manometrisch (wie oben beschrieben) gemessen (DIN EN ISO 14240-1:2011). Die Druckänderung in den ersten 3 Stunden wird nicht in die Auswertung einbezogen, weil sich hier erst ein thermisches Gleichgewicht einstellt. Die Bodenatmung läuft dann ca. 6 Stunden linear bis die Vermehrung der Mikroorganismen einsetzt.
Mittels der Daten aus dem Substrat-induziertes Respirationsverfahren wird die mikrobielle Biomasse in den Bodenproben bestimmt. Die Berechnung erfolgt nach der Gleichung X = 40 R + 0,37 (X = Masse des Cmik im Boden [mg CO2/kg TM]; R = CO2-Bildung [ml CO2/kg * h–1]).
Nitrat wird im Boden zu einem großen Teil durch die Aktivität von Bakterien des Genus Nitrosomas und Nitrobacter gebildet. Bei einem pH-Wert > 5,5 sind diese chemoautotrophen Bakterien für die Nitrifikation in Böden verantwortlich (Foch und Verstraete, 1977). Durch den Einsatz von Natriumcholat als Hemmstoff der Nitrat-Bildung ist es möglich, die Nitrifikation im Kurzbebrütungsversuch (Belser und Mays, 1980) zu bestimmen. NaClO3 hemmt spezifisch Nitrobacter sp. während Nitrosomas europea dagegen nicht beeinflusst wird. Auf Grund der kurzen Inkubationszeit von 6 Stunden kann der Einfluss der Ammonifikation vernachlässigt werden (Berg und Roswall, 1985). Die Rate der Ammoniumoxidation wird in ng NO2/g Boden TM * h–1 angegeben (E DIN ISO 15685).
Cmik/Corg-Verhältnis. Das Cmik/Corg-Verhältnis gibt an, wie hoch der Anteil des in der mikrobiellen Biomasse gebundenen Kohlenstoffs am gesamten organischen Kohlenstoff ist. Dieser Parameter liefert Hinweise auf die Kohlenstoff-Dynamik eines Bodens und zeigt an, in welchem Maß die Bodenmikroorganismen die vorhandenen Kohlenstoffverbindungen zum Aufbau und zur Erhaltung ihrer Lebendmasse nutzen können. Bei langjähriger gleicher Bewirtschaftung stellt sich ein Gleichgewicht zwischen mikrobiellem und organischem Kohlenstoff ein (Anderson und Domsch, 1989). Dieses Cmik/Corg-Verhältnis gilt als annähernd konstant (Haider, 1996). Eine starke Abweichung des Cmik/Corg-Verhältnisses weist auf eine Schädigung der mikrobiellen Biomasse hin (Kandeler et al., 1998).
Metabolischer Quotient (qCO2). Der metabolische Quotient wird aus dem Verhältnis zwischen Basalatmung, genauer gesagt aus dem Kohlenstoffanteil des veratmeten CO2 und der mikrobiellen Biomasse, errechnet. Er wird angegeben in mg CO2-C h–1/g Cmik Der metabolische Quotient stellt einen wichtigen physiologischen Parameter zur Charakterisierung der mikrobiellen Biomasse dar und ist ein indirektes Maß für die energetische Effizienz der Substratnutzung einer Mikroorganismengesellschaft. Er erlaubt Aussagen über den Einfluss anthropogener und natürlicher Faktoren auf die Biomasse und mikrobielle Aktivitäten. Je niedriger der metabolische Quotient, umso geringer sind die C-Verluste durch Veratmung der organischen Bodensubstanz und desto mehr Substrat wird in die mikrobielle Biomasse inkorporiert (Schinner und Sonnleitner, 1996).
Zur statistischen Analyse der Daten wurde das System SAS® Version 9.3 genutzt. Die Mittelwertevergleiche zwischen Prüfglied und Kontrolle erfolgten mit der Prozedur GLM.
Tab. 2 zeigt die – in Laboruntersuchungen – bestimmten und Tab. 3 die berechneten Parameter der mikrobiellen Aktivität in ausgewählten Prüfböden weinbaulich bewirtschafteter Flächen und den zugeordneten Kontrollen.
Es zeigte sich, dass die ausgewählten Kontrollen nicht immer optimal zu den untersuchten Prüfflächen passten. Im Falle des Kontrollbodens MO_06 kam es zu einer nicht zu klärenden Störung bei der Bestimmung der potentiellen Nitrifizierung. Auch bei der Wiederholung des gesamten Versuches wurde ein negatives Ergebnis erzeugt. Der bestimmte pH-Wert für den Boden lag bei 5. In der Kontrolle des Betriebes BA_01 war die potentielle Nitrifizierung, gemessen durch das Schnellverfahren mittels Ammoniumoxidation sehr hoch. Die anderen Parameter wie Atmung und Dehydrogenase-Aktivität zeigten aber ein vergleichbares Verhalten zur Prüffläche.
Die berechneten Parameter der mikrobiellen Biomasse, des metabolischen Quotienten und des Cmik/Corg-Verhältnisses zeigen ein uneinheitliches Bild.
Der metabolische Quotient (qCO2) ist besonders gut geeignet als Indikator bei kurzzeitigen Veränderungen der Umwelt oder Kontaminationen. Da wir aber Böden untersuchten, die z.T. eine 100jährige Bewirtschaftungshistorie (und damit eine langjährige und langsam gestiegene Belastung mit Schwermetallen) aufwiesen, sind bis auf Böden, die einen qCO2 > 9,0 haben, keine signifikanten Abweichungen (s. Tab. 3) im Vergleich zu den Kontrollen festzustellen. Bei den Böden aus der Region Mosel trifft das jeweils bei denen zu, die die höchsten Gesamtgehalte an Kupfer (> 200 mg Cu/kg TM) enthielten und den geringsten Anteil an organischer Substanz. Die ansonsten sehr niedrigen Quotienten in den anderen Böden weisen auf keine signifikanten Effekte bei der Veratmung der organischen Bodensubstanz und damit einhergehender C-Verluste hin.
Sehr starke Unterschiede des Cmik/Corg-Verhältnisses im Vergleich Prüffläche und Kontrollfläche würden auf eine nachhaltige Beeinflussung der Kohlenstoff-Dynamik und Schädigung der mikrobiellen Biomasse eines Bodens hinweisen. Wie in Tab. 2 und 3 gezeigt, sind aber gerade die Böden auffällig, die nicht unbedingt einen hohen Gehalt an Gesamtkupfer aufweisen. Diese Auswirkungen sind sehr gut bei den beiden Betrieben BA_01 und MO_03 zu sehen, bei denen es möglich war, zwei in ihrer Bodencharakteristik vergleichbare Prüfflächen mit unterschiedlich hohen Gesamtgehalten an Kupfer zu untersuchen. Obwohl eine Fläche bis zum 8-fachen der Cu-Konzentration der anderen aufwies, waren bei BA_01 die mikrobiellen Parameter vergleichbar, bei den Prüfböden von MO_03 aber deutlich verschieden.
Auch die in den Prüfböden bestimmten mikrobiellen Parameter zeigen deutlich die Heterogenität der untersuchten Böden. Ein Zusammenhang zwischen steigendem Kupfergehalt und nachhaltiger Beeinflussung der Aktivität der Mikroorganismen in den untersuchten Böden konnte nicht gefunden werden.
In der Literatur, die sich mit der Prüfung und Bewertung der Toxizität von Kupfer in Böden oder Bodensubstraten beschäftigt, ergibt sich bei der Auswertung ein unklares Bild. Das liegt u.a. daran, dass es z. Zt. keine allgemein anerkannte Methode zur Bestimmung dieser Schwermetall-Konzentrationen gibt, die für Bodenmikrooganismen bioverfügbar sind. Bei vielen älteren Studien fehlen die Angaben zur Verfügbarkeit, eine Dosis-Wirkungsbeziehung und Angaben zu physiko-chemischen Bodeneigenschaften der verwendeten Böden/Substrate. Es wurden auch keine standardisierten Methoden verwendet, was die Vergleichbarkeit erschwert. Neuere Studien, die sich mit dem Einfluss von Zn, Cu, Ni und Co auf Mikroorganismen (Oorts et al., 2006a), Invertebraten (Criel et al., 2008) und Pflanzen (Li et al., 2009) beschäftigen und standardisierte Methoden nutzen, lassen als Erklärung für die Variabilitätsbreite der Ergebnisse die Schlussfolgerung zu, dass die Kationenaustauschkapazität im engen Zusammenhang mit dem Boden-pH, Lehmgehalt und Anteil organische Substanz die unterschiedliche Schwermetalltoxizität erklären kann (Wang et al., 2008; Thakali et al., 2006, Oorts et al., 2006b). Die Metalltoxizität sinkt linear mit steigender Kationenaustauschkapazität, dies beschrieben Smolders et al. (2009) in ihren Untersuchungen.
Auch die Art des applizierten Kupfers (als Salz, als Kompost oder in flüssigen Klärschlemmen) beeinflusst die Bioverfügbarkeit entscheidend (Giller et al., 2009).
Wakelin et al. (2010) untersuchten den Zusammenhang zwischen steigendem Gehalt an Kupfer (als CuSO4 appliziert), der Zusammensetzung der Mikroorganismengesellschaft und der Aktivität beim Abbau von organischem Material in einem 6-jährigen Freilandversuch. Sie fanden keinen Zusammenhang zwischen Effekten auf die Basalatmung und steigenden Kupfergehalten (von 0 bis 3225 mg Cu/kg Boden TM). Das liegt einerseits daran, dass die Bioverfügbarkeit von Kupfer eine große Rolle spielt. Die Prozesse der sogenannten Alterung verringern eine mögliche Toxizität gegenüber den Mikroorganismen. Die physiko-chemischen Eigenschaften der Böden (z.B. Korngrößenverteilung, organischer Kohlenstoffgehalt, Kationenaustauschkapazität, pH-Wert) bestimmen das Maß der Auswirkungen auf die Aktivitäten und Leistungen der Bodenmikroorganismen.
Andererseits wurden den Böden keine Mikroorganismen zugesetzt. Es wurde nur mit den in den Böden vorhandenen Populationen getestet. Diese Populationen hatten z.T. 50 Jahre und länger Zeit, sich den steigenden Cu-Gehalten anzupassen.
Wang et al. (2007a) beschrieben dagegen eine negative Korrelation zwischen mikrobieller Biomasse und erhöhtem Cu-Gehalt.
Weiter lassen sich die Effekte ohnehin nicht nur mit einer erhöhten Kupferkonzentration beschreiben. Untersuchungen ergaben, dass auch andere Metalle in durchaus hohen Konzentrationen im Boden bestimmt wurden und bioverfügbar waren (Steindl et al., 2011). So wurde zum Beispiel ein erhöhter Gehalt von Zink durch das Nutzen von Zn-Stickeln für die Befestigung der Weinreben erklärt. Weitere bestimmte Elemente wurden wahrscheinlich mit den früher üblicherweise eingesetzten wasserlöslichen Holzschutzmitteln auf Salzbasis (Arsen-, Chromverbindungen) und Pflanzenschutzmitteln (z.B. Schweinfurter Grün) eingebracht. Ob aber eine Einzelwirkung durch Kombinationseffekte mehrerer Elemente übertroffen wird, ist in der Literatur nicht eindeutig belegt (Malkomes, 2010a).
Die Herkunft und Heterogenität der Böden macht es schwierig, nur die Effekte von Kupfer auf die jeweiligen kurz- oder längerfristigen Endpunkte der Prüfverfahren zu bestimmen. Es ist bei der Probenahme in den ausgewählten Winzerbetrieben nicht immer gelungen, eine geeignete Kontrolle mit vergleichbaren Bodeneigenschaften und Bodenleben zu finden. Das lag daran, dass die Probenahme gezielt für das Regenwurmmonitoring durchgeführt wurde. In den Tests kamen deshalb auch immer sogenannte Kontroll- oder Referenzböden (K_73 und LAGD) aus dem Dahlemer Versuchsfeld mit langjähriger Erfahrung über deren Wirkverhalten zum Einsatz, u.a. um zu überprüfen, wie sich die Testorganismen während der Prüfungen verhalten. Bei Durchführung der Laborversuche zu den unterschiedlichen Zeitpunkten waren die bestimmten Parameter der mikrobiellen Aktivitäten in diesen Böden vergleichbar.
Der Vergleich der Böden von den untersuchten Prüfflächen und den Kontrollen ist in Tab. 4 dargestellt. Zum besseren Verständnis und Vergleich enthält die Tabelle auch die für den jeweiligen Boden bestimmten Gesamtgehalte an Kupfer und den Gehalt an organischer Substanz.
Tab. 4. Mittelwertvergleich mikrobieller Parameter in Prüfböden von Qualitätsweinbaubetrieben mit den Kontrollen, geordnet nach Kupfer-Gesamtgehalten
Betriebe | BA_01 | MO_03 | RH_06 | PF_02 | RH_04 | PF_03 | BA_02 | Mo_03 | Ba_01 | MO_06 | |
Gesamt-Gehalt | PF1 | 28 | 29 | 38 | 74 | 133 | 179 | 186 | 228 | ||
[mg Cu/kg TM] | PF2 | 212 | 225 | ||||||||
| KO | 88 | 20 | 26 | 48 | 18 | 29 | 25 | 20 | 88 | 23 |
org. Substanz | PF1 | 8,4 | 3,9 | 5,2 | 12,1 | 10,2 | 5,1 | 8,1 | 6,6 | ||
[%] | PF2 | 6,4 | 8,6 | ||||||||
| KO | 8,7 | 4,8 | 6,7 | 8,6 | 9,4 | 7,7 | 5,1 | 4,8 | 8,7 | 4,2 |
Statistisch signifikanter Unterschied zur | |||||||||||
Prüfverfahren | Dunnetts einseitige t-Test | ||||||||||
% zur Kontrolle | |||||||||||
Basalatmung | 128 | 265 | 97 | 97 | 159 | 93 | 113 | 77** | 120 | 96 | |
Substratinduzierte | 66** | 52** | 133 | 98 | 120 | 91 | 95 | 120 | 23** | 132 | |
Metabolische Quotient | 198 | 209 | 77 | 98 | 127 | 93 | 115 | 66** | 176 | 74** | |
Cmik/Corg-Verhältnis | 60 | 33** | 96 | 101 | 136 | 64** | 172 | 159 | 38 | 206 | |
Dehydrogenase-Aktivität | 94 | 38** | 99 | 152 | 90** | 103 | 122 | 119 | 98 | 123 | |
Mikrobielle Biomasse | 64** | 43** | 124 | 98 | 125 | 103 | 98 | 119 | 52** | 130 | |
Potentielle Nitrifikation | 9** | 102 | 69** | 107 | 107 | 108 | 50** | 32** | 8** | n. b. | |
* Signifikanzen grau unterlegt; n.b. = nicht bestimmt | |||||||||||
Die im Vergleich zum Kontrollboden signifikanten Unterschiede (DUNNETTS einseitige t-Test mit p ≤ 0,05) lassen sich keiner erhöhten Konzentration an Gesamt-Cu im Boden zuordnen. Eine gesicherte Korrelation mit anderen (Boden-)Parametern lässt sich z.Zt. auf Grund der bisher geprüften 8 Betriebe noch nicht durchführen. Die Situation kann sich verbessern, wenn – wie geplant – noch weitere Betriebe beprobt werden.
Eine zum Teil über Jahrzehnte adaptierte Mikroflora kann ebenfalls eine allgemeine Aussage erschweren. Das Problem bei der Bestimmung der Metall-Toxizität gegenüber Mikroorganismen im Boden ist, dass nachhaltige Auswirkungen auf Stämme einer bestimmten Art, oder auf andere Arten oder Gattungen von Mikroorganismen, die eine bestimmte Funktion im Habitat ausüben, leicht übersehen werden, wenn eine Spezies ersetzt oder deren Funktion von anderen übernommen wird.
Auch die Qualität des vorhandenen oder zugegebenen Substrates zur C-Mineralisierung ist mitentscheidend für die Sensibilität gegenüber einer Kupferkontamination (Giller et al., 1998).
Ge und Zhang (2011) fanden durch Analyse der mikrobiellen Populationen mittels Profile und Indikatoren der Phospholipidfettsäuren (PLFA) und Multiplex-terminalen Restriktions-Fragment-Längen-Polymorphismus (M-TRFLP) Fingerprinting-Verfahren bei gleichzeitiger Analyse der Vielfalt und Community-Struktur, dass Pilze eher und deutlicher auf Kupfer reagieren als Bakterien und Archaeen. Dabei sanken die PLFA-Indikatoren für Gram-positive Bakterien (16:0i, 15:0i) und Pilze (18:2w6,9) mit steigender Cu-Konzentration, während die Indikatoren für Gram-negative Bakterien (19:0cy, 16:1w7) anstiegen. Die pilzliche Gemeinschaft war sensibler als Bakterien und Archaeen. Ranjard et al. (2006) fanden, dass eine Cu-Konzentration von weniger als 20–60 μg g–1 die Zusammensetzung der mikrobiellen Gemeinschaft schon verändern kann. Eine höhere Cu-Konzentration (1000 μg g–1) wurde als ein Schwellenwert für toxische Wirkungen auf der Grundlage von PLFA Profile (Bååth et al., 1998) beschrieben. Aufgrund der PLFA und bakterielle TRFLP Ergebnisse wurden Grenzwerte für die Toxizität im Boden vorgeschlagen, die zwischen 351–708 μg g–1 total Cu oder 126–184 μg war g–1 verfügbares Cu lagen. Setzte man die pilzlichen TRFLP Profile als Maßstab, wurden niedrigere Schwellenwerte gefunden (170–351 μg g–1 total Cu oder 50–126 μg g–1 verfügbares Cu).
In dieser Arbeit wurde bisher auf die im Zulassungsverfahren geforderten Parameter eingegangen. Für eine bessere Erklärung der Phänome müssen aber auch Methoden gewählt werden, die z.B. eine Verschiebung der Biodiversität der Populationen von Mikroorganismen erfassen können.
Dell´Amico et al. (2008) bestätigten diesen Effekt in ihren Untersuchungen von zwei Weingärten im Piemont, Nord-Italien. Zwar war an beiden Standorten der Anteil Cu-toleranter Bakterien hoch, doch herrschten im geringer mit Cu belasteten Boden gram-positive Bakterien vor, im höher belasteten dagegen gram-negative.
Ein Problem vieler Untersuchungen über den Einfluss von Kupfer ist, das der Boden vor Beginn der Untersuchungen erst mit Kupfer oder Gemischen von Schwermetallen versetzt wurde. (Chandler et al., 1995; Wilke et al., 2005). Zu dieser Zeit ist die Bioverfügbarkeit relativ hoch und damit verbunden die toxische Wirkung. Für die Zulassung von Pflanzenschutzmitteln ist dieser „worst case“ gut geeignet, mit dem Wissen, dass es im Freiland solche Bedingungen nicht gibt und hier eine Art Sicherheitsfaktor eingebaut wird. Nach Ausbringen kupferhaltiger Präparate wird das Schwermetall relativ schnell an Tonminerale oder organische Substanz gebunden und ist nicht mehr im hohen Maße bioverfügbar.
So untersuchten Wightwick et al. (2013) Weinbergsböden in Mikrokosmosanlagen im Labor. Der Boden stammte aus den oberen 5 cm. Die Kontrollen wurden ganz in der Nähe genommen mit geringem oder keinem zusätzlichen Kupfer. Die untersuchten Parameter waren Phosphomonoesterase-, Arylsulfatase-, Urease- und Phenoloxidase-Aktivität. Nur bei der Phosphomonoesterase-Aktivität fanden sie eine geringe Abhängigkeit zum Cu-Gehalt.
Aus den gemessenen Werten, z.B. der Bodenatmung (LZA und SIR), lassen sich weitere ökophysiologische Parameter zur Beurteilung der Effekte auf die Bodenmikroorganismen ableiten. Diese sind zum Teil weniger durch Einflüsse der Bodenbewirtschaftung oder Zusatzbepflanzung beeinflusst als die ihnen zugrunde liegenden Einzelparameter. Trotzdem kann man mit ihnen die Qualität und Quantität von Umsetzungsprozessen beschreiben.
In der Abb. 1 sind die Verhältnisse bei den untersuchten Prüf- und Kontrollflächen grafisch dargestellt. Ein höheres Cmik/Corg-Verhältnis verdeutlicht eine effektivere Ausnutzung der organischen Substanz zum Aufbau mikrobieller Biomasse. Neben verschiedenen Eigenschaften der Mikroorganismen und den sie beeinflussenden Umweltbedingungen ist hierfür die Qualität der organischen Substanz wichtig (z.B. leicht oder schwer abbaubar, N-Gehalt). Die organische Substanz der Prüfflächen wurde aber nicht in ihrer speziellen Zusammensetzung untersucht.
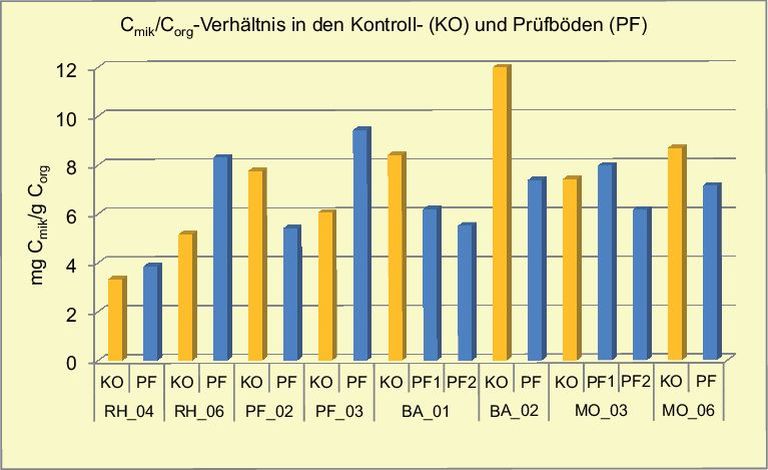
Abb. 1. Cmik/Corg-Verhältnis in den Prüfböden im Vergleich zur Kontrolle.
Cmic/Corg-ratio in the test soils compared to controls.
Eine leicht verfügbare Nahrungsquelle kann die Entwicklung der mikrobiellen Biomasse steigern, wohingegen die Zufuhr bereits humifizierten organischen Materials (z.B. gealterter Kompost oder Stallmist) eher den Humusgehalt des Bodens fördert und somit das Cmik/Corg-Verhältnis tendenziell erniedrigt (Reuter, 1999; Reuter und Kubiak, 2001). Laut Aussage der Winzer wurden kurz vor dem Zeitpunkt der Probenahme keine dieser Maßnahmen in den Weinbergen durchgeführt. Eine deutliche Störung der mikrobiellen Umsetzungsprozesse konnte nicht beobachtet werden. Bei den Prüfböden BA_01 und MO_03 mit den jeweils unterschiedlich hohen Kupfer-Gesamtgehalten wurden keine Unterschiede des Cmik/Corg-Verhältnisses festgestellt.
Im Gegensatz dazu beschrieben Bååth et al. (1991) und Fliessbach et al. (1994), dass Metallkontaminationen die Ratio senken. Bei anderen Untersuchungen (Insam et al., 1996) konnten keine Unterschiede zwischen kontaminierten und unkontaminierten Böden festgestellt werden. Ihrer Meinung nach überdeckten andere Parameter wie unterschiedliche Bodeneigenschaften, Textur, pH-Wert und Corg-Gehalt die Ausprägung. Wie schon bei den Modellböden gezeigt, ist auch bei den Prüfböden der Cu-Gehalt nicht entscheidend.
Auch der metabolische Quotient (qCO2) als indirektes Maß für die energetische Effizienz einer Mikroorganismengesellschaft kann bei einer Erhöhung als Hinweis z.B. auf Stresswirkungen gesehen werden (Anderson und Domsch, 1986b). Unter Stress wird ein höherer Anteil der umgesetzten Energie für lebenserhaltende Prozesse benötigt, so dass Wachstumsprozesse eine Reduzierung erleiden können. Außer dem – lange Zeit trocken gelagerten – Kontroll- und Referenzboden LAGD sind die Kohlenstoff-Verluste der Modellböden durch Veratmung der organischen Bodensubstanz gering. Es ist keine Störung der Substrateinlagerung in die mikrobielle Biomasse zu beobachten.
Die berechneten metabolischen Quotienten der Prüfböden (Tab. 3) zeigen ein indifferentes Bild. Sie geben keine Hinweise auf eine negative Auswirkung bzw. eine Stresswirkung bedingt durch einen erhöhten Gesamtgehalt an Kupfer. Die unterschiedlichen Niveaus der einzelnen Weinbauregionen bringen nur zum Ausdruck, dass die jeweiligen Standorte ganz spezifische Bodencharakteristika, Klima und Habitate aufweisen, die alle auf die Diversität und Abundanz der Populationen von Mikroorganismen einwirken.
Fliessbach et al. (1994) und Moreno et al. (1999) beobachteten eine Erhöhung des metabolischen Quotienten in Böden, die mit Schwermetallen kontaminiert wurden. Diese gesteigerten Metabolismusraten erklärten sie mit einer unspezifischen Reaktion auf die veränderten Umweltbedingungen und als Stressantwort (Selye, 1950). Die Situation in den Weinbergsböden ist insofern anders, als hier die sukzessive Belastung mit Kupfer über einen langen Zeitraum erfolgte, das Kupfer zum Teil festgelegt wurde und eine Toleranz bzw. Adaption durch die Mikroorganismen aufgebaut werden konnte. Das zeigt sich darin, dass Bodenenzyme durch eine moderate Anwendung von Kupfer nicht oder kaum beeinträchtigt werden (Macdonald et al., 2007).
Auch die durch Ge und Zhang (2011) gemessene Phosphatase-Aktivität war nicht signifikant durch Schwermetallkontamination beeinflusst.
Bei einigen mikrobiellen Aktivitäten lagen die EC50-Werte für Cu im Boden meistens deutlich höher als der erlaubte jährliche Cu-Eintrag und betrugen z.B. 259 mg/kg (Basalatmung), von 95 bis 850 mg/kg (SIR), von 95 bis 825 mg/kg (Abbau von Maisrückständen), von 73,4 bis 2060 mg/kg (potenzielle Nitrifikation), 150 mg/kg (Dehydrogenaseaktivität), 285 mg/kg (Abbau organischer Substanz). Doch sollten diese Angaben wegen zahlreicher ebenfalls vorliegender niedrigerer Werte aus anderen Untersuchungen zunächst nicht verallgemeinert werden (Malkomes, 2010b).
Andererseits gibt es auch genügend Beweise, die dokumentieren, dass eine Abnahme der Enzymaktivität im Boden ein Ergebnis der langfristigen Exposition gegenüber Schwermetallbelastung ist (Wang et al., 2007b; Speir et al., 2007). An 99 unterschiedlich stark mit Schwermetallen einschließlich Cu (6,4–497 mg/kg TM) belasteten Schweizer Freilandböden, darunter 61 Acker- und 9 Weinbergsböden, ermittelten Celardin und Chatenoux (2003) u.a. die mikrobielle Biomasse (ATP-Gehalt) und die Basalatmung (CO2-Bildung über 15 d). Sowohl die Biomasse als auch besonders die Atmung nahmen dosisabhängig mit dem Cu-Gehalt im Boden ab, wobei die EC50-Werte für die Atmung bei etwa 259 mg Cu/kg Boden TM lagen. Ein von Wilke et al. (2005) durchgeführter Vergleich von SIR-Atmungskurven nach Glucosezugabe ergab ab etwa 190 mg Cu/kg Boden TM eine deutlich empfindlichere Reaktionen in den frisch mit CuCl2 versetzten Böden als in den die entsprechenden Mengen gealterter Cu-Rückstände enthaltenden Böden.
Oorts et al., 2006b verglichen die Wirkung auf die SIR in frisch mit Cu-Salzen (Carbonat, Chlorid, Sulfat) versetzten Böden mit der Aktivität in entlang eines Cu-Konzentrationsgradienten entnommenen „gealterten“ Proben. Es ergaben sich EC50-Werte im Bereich von 95 bis > 850 mg Cu/kg Boden TM. Dabei erwiesen sich je nach Boden teilweise die frisch kontaminierten Proben als empfindlicher, teilweise aber auch die anhand eines Cu-Gradienten im Feld entnommenen gealterten.
In einigen Fällen scheint eine lang anhaltende und langsam in der Konzentration steigende Cu-Belastung in Böden zusätzlich die Entstehung Cu-toleranterer mikrobieller Populationen zu ermöglichen (Kamitani et al., 2006).
Seit längerem ist bekannt (Behlau et al., 2012; Lee et al., 1994; Cooksey und Azad, 1992), dass bei Anwendung von Kupfer-haltigen Bakteriziden sich Cu-resistente Stämme entwickeln können. Dies können Spezies sein von Pseudomonaden (Bender und Cooksey, 1986), Pantoea (Nischwitz et al., 2007), Erwinia (Al-Daoude et al., 2009) und Xanthomonaden (Marco und Stall, 1983). Der Mechanismus der Resistenz wird erklärt durch die Akkumulation und Festlegung von Kupfer in den Bakterienzellen mit Hilfe von Proteinen. Der horizontale Transfer ist hauptsächlich verantwortlich für die Weitergabe dieser Eigenschaft an andere Bakterien. Eine Spontanmutation kann fast ausgeschlossen werden, da die Regulierung der Kupferresistenz über mehrere Gene im Organismus erfolgt (Cooksey, 1990). Auch die Mechanismen der Toleranz in Bakterien und Pilzen sind sehr vielfältig. Hierbei wird der Begriff Toleranz nach den Empfehlungen von Gadd (1992) genutzt für Fälle, wo ein Entgiftungsmechanismus die Fähigkeit verleiht, unter Bedingungen des Schwermetall-Stresses zu überleben. Diese Mechanismen können sein: Bindung des Metalls durch Proteine, extrazelluläre Polymere oder die Zellwand, Kompartimentierung innerhalb der Zelle, Bildung unlöslicher Metallsulfide, verminderte Aufnahme, verbesserte Freisetzung aus Zellen und Volatilation (Silver und Misra, 1988; Flemming und Trevors, 1989; Cooksey, 1993; Ross, 1993).
Die Prüfung des Einflusses von Kupfer auf Parameter der Bodenmikroorganismen weist auf einen ungestörten Ein- und Umbau der mikrobiellen Biomasse hin. Entweder tolerieren die Bodenmikroorganismen den hohen Kupfergehalt und haben sich an die Bedingungen adaptiert oder die Diversität ist groß genug, dass die Funktionen und Enzymaktivitäten der von Kupfer beeinflussten Mikroorganismen durch andere Arten oder Gattungen ersetzt werden können. Methodisch hat es sich als problematisch erwiesen, dass die am Standort zur Verfügung stehenden Kontrollflächen z.T. nicht immer mit den in Nutzung stehenden Prüfflächen vergleichbar waren (für die mikrobiologischen Untersuchungen). Hier ist schwer zu interpretieren, welche anderen Parameter die Effekte am stärksten beeinflussen.
Ein weiteres Problem bei Freilanduntersuchungen ist die Mehrfachbelastung z.B. mit anderen Schwermetallen (Strumpf et al., 2011). Hier war – methodisch – keine saubere Trennung der Effekte möglich. Vereinzelt sind in den Weinbergsböden Gesamt-Konzentrationen anderer Metalle gemessen worden, die ebenfalls toxische Effekte bei den Mikroorganismen hervorrufen können. Auch aus der Literatur ist diese Schwierigkeit bekannt. Freilanduntersuchungen nur mit einzelnen Schwermetallbelastungen gibt es kaum.
In dieser Arbeit nicht näher untersucht wurden Einflüsse auf die Diversität der Bodenmikroorganismen. Funktions- und Summenparameter können nicht immer eindeutig zeigen, ob es zu nachhaltigen Auswirkungen gekommen ist. Zum Teil überlagern sich positive und negative Effekte.
Bei einem langfristigen und langsamen Anstieg der Gesamtkonzentration nach Anwendung kupferhaltiger PSM muss damit gerechnet werden, dass sich Cu-resistente Populationen von Mikroorganismen entwickeln und aufbauen können (Brandt et al., 2010). Dieses würde auch die große Differenz bei den Angaben über schädigende Cu-Konzentrationen erklären.
Bei der Prüfung der Böden wurde von den gesetzlich geforderten Untersuchungen bei der Bewertung im Rahmen der Zulassung von PSM ausgegangen und die geforderten Prüfungen zur Beeinflussung der Mikroorganismen im Boden durchgeführt. Nachhaltige Effekte durch hohe Kupferkonzentration auf die bestimmten mikrobiellen Aktivitätsparameter konnten hierbei nicht festgestellt werden. Dies bedeutet aber nicht, dass die Mikroorganismengesellschaften im Boden nicht auf die erhöhten Schwermetallgehalte reagieren. Hierzu sind weitere Untersuchungen notwendig.
Der Autor dankt für die Durchführung der Laboruntersuchungen Frau Bärbel Flessner, Frau Martina Blossfeld, Frau Sylvia Baas und Frau Elke Reich. Weiterhin danken die Autoren Frau Ursula Stendel, Frau Martina Kulcke und Frau Catrin Vetter für ihre technische Assistenz bei der Extraktion und Bestimmung der Cu-Gehalte und der physiko-chemischen Basisparameter der gesammelten Qualitätsweinbaubodenproben. Vielen Dank auch an Herrn Dr. Thomas Strumpf für die wertvollen Hinweise beim Erstellen dieser Arbeit.
Anderson, T.H., K.H. Domsch, 1986a: Carbon assimilation and microbial activity in soil. Zeitschrift für Pflanzenernährung und Bodenkunde 149, 457-468.
Anderson, T.H., K.H. Domsch, 1986b: Anwendung ökophysiologischer Parameter zur Charakterisierung mikrobieller Biomassen im Boden. In: Riewenherm, S., H. Lieth (Hrsg.). Verhandlungen der Gesellschaft für Ökologie, 19/II, 324-329.
Al-Daoude, A., M.I.E. Arabi, H. Ammouneh, 2009: Studying Erwinia amylovora isolates from Syria for copper resistance and streptomycin sensitivity. Journal of Plant Pathology 91, 203-205.
Anderson, T.-H., K.H. Domsch, 1989: Ratios of Microbial Biomass Carbon to Total Organic Carbon in Arable Soils. Soil Biology and Biochemistry, 21, 471-479.
Bååth, E., K. Arnebrandt, A. Nordgren, 1991: Microbial biomass and ATP in smelter-polluted forest humus. Bulletin of Environmental Contamination and Toxicology 47, 278-282.
Bååth, E., M. Diaz-Ravina, A. Frosteg˚ard, C.D. Campbell, 1998: Effect of metal-rich sludge amendents on the soil microbial community. Applied and Environmental Microbiology 64, 238-245.
BBodSchV, 1999: Bundes-Bodenschutz- und Altlastenverordnung (BBodSchV). Neufassung vom 12.07.1999.
Behlau, F., J.C. Hong, J.B. Jones, J.H. Graham, 2012: Evidence for Acquisition of Copper Resistance Genes from Different Sources in Citrus-Associated Xanthomonads. Phytopathology 103 (5), 409-418.
Belser, L.W., E.L. Mays, 1980: Specific inhibition of nitrite oxidation by cholate and its use in assessing nitrification in soils and sediments. Applied and Environmental Microbiology 39, 505-510.
Bender, C.L., D.A. Cooksey, 1986: Indigenous plasmids in Pseudomonas syringae pv. tomato: Con jugative transfer and role in copper resistance. Journal Bacteriology 165, 534-541.
Berg, P., T. Roswall, 1985: Ammonium oxidizer number, potential and actual oxidation rates in two Swedish arable soils. Biology and Fertility of Soils 1, 131-140.
Bertrand, I., L.J. Janik, R.E. Holloway, R.D. Armstrong, M.J. McLaughlin, 2002: The rapid assessment of concentrations and solid phase associations of macro- and micronutrients in alka-line soils by mid-infrared diffuse reflectance spectroscopy. Australian Journal of Soil Research 40 (8), 1339-1356.
Brandt, K., R.J.N. Frandsen, P.E. Holm, O. Nybroe, 2010: Development of pollution-induced community tolerance is linked to structural and functional resilience of a soil bacterial community following a five-year field exposure to copper. Soil Biology and Biochemistry 42, 748-757.
Brookes, P.C., 1995: The use of microbial parameters in monitoring soil pollution by heavy metals. Biology and Fertility of Soils 19, 269-279.
Chandler, K., P.C. Brookes, 1991: Is the dehydrogenase assay invalid as a method to estimate micro bial activity in copper contaminated soils? Soil Biology and Biochemistry 23, 909-915.
Chandler, K., P.C. Brookes, S.A. Harding, 1995: Microbial biomass dynamics following addition of metal-enriched sewage sludges to a sandy loam. Soil Biology and Biochemistry 27 (11), 1409-1421.
Celardin, F., L. Chatenoux, 2003: Correlations between soil microbiological parameters (CO2 respiration, ATP-biomass) and heavy metals in field soils. Archives des sciences, Genève 56 (3), 127-135.
ChemG, 2008: Gesetz zum Schutz vor gefährlichen Stoffen (Chemikaliengesetz – ChemG) Neufassung vom 02.07.2008.
Clemens, S., 2001: Molecular mechanisms of plant metal tolerance and homeostasis. Planta 212, 475-486.
Cooksey, D.A., 1990: Genetics of bactericide resistance in plant pathogenic bacteria. Annual Reviews Phytopathology 28, 201-219.
Cooksey, D.A., 1993: Copper uptake and resistance in bacteria. Molecular Microbiology, 7, 1-5.
Cooksey, D.A., H.R. Azad, 1992: Accumulation of copper and other metals by copper-resistant plant-pathogenic and saprophytic pseudomonads. Applied Environmental Microbiology 58, 274-278.
Covelo, E.F., F.A. Vega, M.L. Andrade, 2008: Sorption and desorption of Cd, Cr, Cu, Ni, Pb and Zn by a fibric histosol and its organo-mineral fraction. Journal of Hazardous Materials 159, 342-347.
Criel, P., K. Lock, H. Van Eeckhout, K. Oorts, E. Smolders, C.R. Janssen, 2008: Influence of soil properties on copper toxicity for two soil invertebrates. Environmental Toxicology and Chemistry 27, 1748-1755.
Dell´Amico, E.M., M. Mazzocchi, L. Cavalca, L. Allievi, V. Andreoni, 2008: Assessment of bacterial community structure in a long-term copper-polluted ex-vineyard soil. Microbiological Research 163, 671-683.
Dick, R.P., D. Breakwill, R. Turco, 1996: Soil enzyme activities and biodiversity measurements as integrating biological indicators. In: Doran, J.W., A.J. Jones (Eds.), Handbook of Methods for Assessment of Soil Quality. Soil Science Society of America Specific Publications, Madison, WI, pp. 242-272.
DIN ISO 11465:1996: Bodenbeschaffenheit – Bestimmung der Trockensubstanz und des Wassergehalts auf Grundlage der Masse – Gravimetrisches Verfahren.
DIN ISO 15685:2004: Bodenbeschaffenheit – Bestimmung der potentiellen Nitrifizierung und Hemmung der Nitrifizierung – Schnellverfahren mittels Ammoniumoxidation (ISO 15685:2004).
DIN ISO 10390:2005: Bodenbeschaffenheit – Bestimmung des pH-Wertes (ISO 10390:2005).
DIN ISO 23753-1:2006: Bodenbeschaffenheit – Bestimmung der Dehydrogenaseaktivität in Böden – Teil 1 Verfahren mit Triphenyltetrazoliumchlorid (TTC) (ISO 23753-1:2005).
DIN ISO 23753-1:2006: Bodenbeschaffenheit – Bestimmung der Dehydrogenaseaktivität in Böden – Teil 2: Verfahren mit Iodotetrazoliumchlorid (ISO 23753-2:2005).
DIN ISO 16072:2011: Bodenbeschaffenheit – Laborverfahren zur Bestimmung der mikrobiellen Bodenatmung (ISO 16072:2002).
DIN ISO 14240-1:2011: Bodenbeschaffenheit – Bestimmung der mikrobiellen Biomasse von Böden – Teil 1: Substrat-induziertes Respirationsverfahren (ISO 14240-1:1997) Deutsche Fassung EN ISO 14240-1:2011.
E DIN ISO 11274: Bodenbeschaffenheit – Bestimmung des Wasserrückhaltevermögens – Laborverfahren (ISO 11274:1998).
Emmerling, C., P. Ritzmann, D. Schröder, 1997: Langzeitwirkung organischer Reststoffe auf bodenbiologische Eigenschaften und den Streuabbau in Weinbergsböden. Mitteilungen Deutsche Bodenkundliche Gesellschaft 85 (II), 679-682.
Fernàndez-Calvino, D., P. Soler-Rovira, A. Polo, M. Diaz-Ravina, M. Arias-Estevez, C. Plaza, 2010: Enzyme activities in vineyard soils long-term treated with copper-based fungicides. Soil Biology and Biochemistry 42, 2119-2127.
Flemming, C.A., J.T. Trevors, 1989: Copper toxicity and chemistry in the environment: A review. Water, Air and Soil Pollution 44, 143-158.
Fliessbach, A., R. Martens, H.H. Reber, 1994: Soil microbial biomass and microbial activity in soils treated with heavy metal contaminated sewage sludge. Soil Biology and Biochemistry 26, 1201-1205.
Foch, D.D., W. Verstraete, 1977: Biochemical ecology of nitrification and denitrification, Advances in Microbial Ecology 1 (1), 35-214.
Gadd, G.M., 1992: Metals and microorganisms: a problem of definition. FEMS Microbiology Letters 100, 197-203.
Ge, C.R., Q.C. Zhang, 2011: Microbial Community Structure and Enzyme Activities in a Sequence of Copper-Polluted Soils. Pedosphere 21 (2), 164-169.
Giller, K.E., E. Witter, S.P. McGrath, 1998: Toxicity of heavy metals to microorganisms and microbe al processes in agricultural soils: a review. Soil Biology and Biochemistry 30, 1389-1414.
Giller, K.E., E. Witter, S.P. McGrath, 2009: Heavy metals and soil microbes. Soil Biology and Biochemistry 41, 2031-2037.
Haider, K., 1996: Biochemie des Bodens. Stuttgart, Ferdinand Enke Verlag, 174 Seiten.
Insam, H., T.C. Hutchinson, H.H. Reber, 1996: Effects of heavy metal stress on the metabolic quotient of the soil microflora. Soil Biology and Biochemistry 28 (415), 691-694.
Li, H.F., C. Gray, C. Mico, F.J. Zhao, S.P. McGrath, 2009: Phytotoxicity and bioavailability of cobalt to plants in a range of soils. Chemosphere 75, 979-986.
Kamitani, T., H. Oba, N. Kaneko, 2006: Microbial biomass and tolerance of microbial community on an aged heavy metal polluted floodplain in Japan. Water, Air and Soil Pollution 172, 185-200.
Kandeler, E., C. Kampichler, O. Horak, 1996: Influence of heavy metals on the functional diversity of soil microbial communities. Biology and Fertility of Soils 23, 299-306.
Kandeler, E., D. Tscherko, G. Wessolek, 1998: Bodenökologie & Bodengenese, Reaktion von Mikroorganismen auf Bodenkontaminationen. Tagungsband: Mobilität und Wirkung von Schadstoffen in urbanen Böden, Heft 26; Februar 1998.
Kozdroj, J., 1995: Microbial responses to single or successive soil contamination with Cd or Cu. Soil Biologie and Biochemistry 27, 1459-1465.
Kratz, S., S. Haneklaus, E. Schnug, 2009: Kupfergehalte in Acker- und Grünlandböden und das Verhältnis dieser Gehalte zu den durch Pflanzenschutz ausgebrachten Kupfermengen. Journal für Kulturpflanzen 61 (4), 112-116.
Lee, Y.A., M. Hendson, N.J. Panapoulos, M.N. Schroth, 1994: Molecular cloning, chromosomal map ping, and sequence analysis of copper resistance genes from Xanthomonas campestris pv. juglandis: Homology with small blue copper proteins and multicopper oxidase. Journal of Bacteriology 176, 173-188.
Macdonald, C.A., B.K. Singh, J.A. Peck, A.P. van Schaik, L.C. Hunter, J. Horswell, C.D. Campbell, T.W. Speir, 2007: Long-term exposure to Zn-spiked sewage sludge alters soil community structure. Soil Biology and Biochemistry 39 (10), 2576-2586.
Malkomes, H.-P., 2010a: Einfluss Kupfer-haltiger anthropogener Einträge auf Bodenmikoorganismen – eine Übersicht. I. Mikrobielle Populationen, Journal für Kulturpflanzen 62 (6), 211-222.
Malkomes, H.-P., 2010b: Einfluss Kupfer-haltiger anthropogener Einträge auf Bodenmikoorganismen – eine Übersicht. II. Mikrobielle Aktivitäten. Journal für Kulturpflanzen 62 (12), 429-443.
Marco, G.M., R.E. Stall, 1983: Control of bacteriaspot of pepper initiated by strains of Xanthomonas campestris pv. vesicatoria that differ in sensitivity to copper. Plant Diseases 67, 779-781.
Moreno, J.L., T. Hernandez, C. Garcia, 1999: Effects of a cadmium contaminated sewage sludge compost on dynamics of organic matter and microbial activity in an arid soil. Biology and Fertility of Soils 28, 230-237.
Nischwitz, C., R. Gitaitis, H. Sanders, D. Langston, B. Mullinex, R. Torrence, G. Boyhan, L. Zolobowska, 2007: Use of fatty acid methyl ester profilest o compare copper-tolerant and copper-sensititve strains of Pantoea ananatis. Phytopathology 97, 1298-1304.
Obbard, P., 2001: Measurement of dehydrogenase activity using 2-piodophenyl-3-p-nitrophenyl-5-phenyltetrazolium chloride (INT) in the presence of copper. Biology and Fertility of Soils 33, 328-330.
Oberholzer, H.R., H. Höper, 2000: Reference systems for the microbiological evaluation of soils, VDLUFA-Schriftenreihe 55; Darmstadt, VDLUFA, pp. 19-34.
OECD-Guideline for Testing of Chemicals, Soil Microorganisms: Nitrogen Transformation Test, Guide line 216 (21.01.2000).
OECD-Guideline for Testing of Chemicals, Soil Microorganisms: Carbon Transformation Test, Guideline 217 (21.01.2000).
Oliveira, A., M.E. Pampulha, 2006: Effects of long-term heavy metal contamination on soil micro-bial characteristics. Journal of Bioscience and Bioengineering 102 (3), 157-161.
Oorts, K., U. Ghesquiere, K. Swinnen, E. Smolders, 2006a: Soil properties affecting the toxicity of CuCl2 and NiCl2 for soil microbial processes in freshly spiked soils. Environmental Toxicology and Chemistry 25, 836-844.
Oorts, K., H. Bronckaers, E. Smolders, 2006b: Discrepancy of the microbial response to elevated Cu between freshly spiked and long-term contaminated soils. Environmental Toxicology and Chemistry 25, 845-853.
PflSchG, 2012: Gesetz zum Schutz der Kulturpflanzen (Pflanzenschutzgesetz – PflSchG) Neufassung vom 06.02.2012.
Ranjard, L., A. Echairi, V. Nowak, D.P.H. Lejon, R. Nouaim, R. Chaussod, 2006: Field and micro-cosm experiments to evaluate the effects of agricultural Cu treatment on the density and genetic structure of microbial communities in two different soils. FEMS Microbiology Ecology 58, 303-315.
Reuter, S., 1999: Relation entre les caractéristiques physiques etbiologiques des sols viticoles et le devenir de deux herbicides, en fonction des changements de pratiques d’entretien des sols. Raport final du stage post-doctorale, Université de Bourgogne, Dijon, CST-Geo Sol.
Reuter, S., R. Kubiak, 2001: Soil management systems to support soil microbial biomass in vineyards. In: Conservation Agriculture, a Worldwide Challenge, vol. II. Garcia-Torres, L., J. Benites, A. Martinez-Vilela. (eds.). Cordoba, XUL, 497-501.
Riepert, F., A. Steindl, R. Eibach, M. Maixner, C. Reichmuth, J. Strassemeyer, T. Strumpf, 2010: Monitoring of total contents of copper in organically and conventionally managed soils. Part 1: Study plan and preliminary sampling of copper and other anthropogenic induced heavy metal contents in vineyard soils, Journal für Kulturpflanzen 62 (2), 42-50.
Riepert, F., D. Felgentreu, T. Strumpf, 2013: Auswirkungen von Kupfereinträgen im Weinbau auf die Regenwurmzönose – Ergebnisse von Feldbeprobungen. Journal für Kulturpflanzen 65 (12), xx.
Ross, I.S., 1993: Membrane transport processes and response to heavy metals. In: Stress Tolerance of Fungi, ed. D.H. Jennings. New York, Marcel Dekker, pp. 97-125.
Rossel, D., J. Tarradellas, G. Bittom, J.-L. Morel, 1997: Use of enzymes in soil ecotoxicology: a case for dehydrogenase and hydrolytic enzymes. In: Tarradellas, J., G. Bitton, D. Rossel (Eds.), Soil Ecotoxicology. Boca Raton, FL, Lewis Publishers, CRC Press, pp. 179-206.
Scheffer, F., P. Schachtschabel, 1982: Lehrbuch der Bodenkunde. Stuttgart, Ferdinand Enke Verlag, S. 281.
Schinner, F., R. Sonnleitner, 1996: Ökophysiologische Parameter. In: Schinner, F., R. Sonnleitner (Hrsg.), Bodenökologie. Mikrobiologie und Bodenenzymatik. Band 1. Berlin (u.a.), Springer, S. 255.
Selye, H., 1950: Stress and the general adaptation syndrome. British Medical Journal 4667, 1383-1392.
Silver, S., K. Misra, 1988: Plasmid-mediated heavy metal resistances. Annual Reviews of Microbiology 42, 717-743.
Smolders, E., K. Oorts, P. Van Sprang, I. Schoeters, C.R. Janssen, S.P. McGrath, M.L. McLaughlin, 2009: The toxicity of trace metals in soil as affected by soil type and ageing after contamination: using calibrated bioavailability models to set ecological soil standards. Environmental Toxicology and Chemistry 28, 1633-1642.
Speir, T.W., A.P. van Schaik, L.C. Hunter, J.L. Ryburn, H.J. Percival, 2007: Attempts to derive EC50 values for heavy metals from land applied Cu-, Ni-, and Zn-spiked sewage sludge. Soil Biology and Biochemistry 39, 539-549.
Steindl, A., T. Strumpf, F. Riepert, 2011: Bioverfügbare Kupfergehalte in ökologisch und konventionell bewirtschafteten Böden deutscher Wein- und Hopfenanbaugebiete. Teil 3: Bestimmung des pflanzenverfügbaren Anteils Kupfer- und anderer Schwermetallgehalte durch NH4NO3-Extraktion. Journal für Kulturpflanzen, 63 (5),156-166.
Strumpf, T., A. Steindl, J. Strassemeyer, F. Riepert, 2011: Erhebung von Kupfergesamtgehalten in ökologisch und konventionell bewirtschafteten Böden. Teil 1: Gesamtgehalte in Weinbergsböden deutscher Qualitätsanbaugebiete. Journal für Kulturpflanzen, 63 (5), 131-143.
Tao, S., Y.J. Chen, F.L. Xu, J. Cao, B.G. Li, 2003: Changes of copper speciation in maize rhizosphere soil, Environmental Pollution 122, 447-454.
Thakali, S., H.E. Allen, D.M. Di Toro, A.A. Ponizovsky, C.P. Rooney, F.J. Zhao, S.P. McGrath, P. Criel, H. van Eeckhout, C.R. Janssen, K. Oorts, E. Smolders, 2006: Terrestrial bioticligand model. 2. Application to Ni and Cu toxicities to plants, invertebrates, and microbes in soil. Environmental Science and Technology 40, 7094-7100.
Van-Zwieten, L., G. Merrington, M. Van-Zwieten, 2004: Review of impacts on soil biota caused by cop per residues from fungicide application. SuperSoil 2004: 3rd Australian New Zealand Soils Conference, 5–9 December 2004, Australia, University of Sydney.
VDLUFA, 1991: Methodenbuch, Band I. Die Untersuchung von Böden, A 2.4.3.1. VDLUFA-Verlag Darmstadt; DIN (1983): DIN 38414, Teil 7. Aufschluss mit Königswasser zur nachfolgenden Bestimmung des säurelöslichen Anteils von Metallen. Berlin, Beuth Verlag.
Wang, Y.P., Q.B. Li, W. Hui, J.Y. Shi, Q. Lin, X.C. Chen, Y.X. Chen, 2008: Effect of sulphur on soil Cu/Zn availability and microbial community composition. J. of Hazardous Materials 159 (2-3), 385-389.
Wang, Y.P., J.Y. Shi, Q. Lin, X.C. Chen, Y.X. Chen, 2007a: Heavy metal availability and impact on activity of soil microorganisms along a Cu/Zn contamination gradient. J. Environmental Sciences-China 7, 848-853.
Wang, Y., J. Shi, H. Wang, Q. Lin, X. Chen, Y. Chen, 2007b: The influence of soil heavy metals pollution on soil microbial biomass, enzyme activity, and community composition near a copper smelter. Ecotoxicology and Environmental Safety 67, 75-81.
Wakelin, S.A., G. Chu, K. Broos, K.R. Clarke, Y. Liang, M.J. McLaughlin, 2010: Structural and functional response of soil microbiota to addition of plant substrate are moderated by soil Culevels. Biology and Fertility of Soils 46, 333-342.
Wightwick, A.M., S.A. Salzmann, S.M. Reichman, G. Allison, N.W. Menzies, 2013: Effect of copper fungicide residues on the microbial function of vineyard soils. Environmental Science and Pollution Research 20, 1574-1585.
Wilbois, K.-P., R. Kauer, B. Fader, J. Kienzle, P. Haug, A. Fritzsche-Martin, N. Drescher, E. Reiners, P. Röhrig, 2009: Kupfer als Pflanzenschutzmittel unter besonderer Berücksichtigung des Ökologischen Landbaus. Journal für Kulturpflanzen 61, 140-152.
Wilke, B.-M., M. Mai, A. Gattinger, M. Schloter, P. Gong, 2005: Effects of fresh and aged copper contaminations on soil microorganisms. Journal of Plant Nutrition and Soil Science 168, 668-675.
Yu, S., Z.L. He, C.Y. Huang, G.C. Chen, D.V. Calvert, 2002: Adsorption-desorption behavior of copper contaminated levels in red soils from China. Journal of Environmental Quality 31, 1129-1136.