

Eine einfache und schnelle lichtmikroskopische Methode zur Identifizierung von Rostpilzen (Puccinia spp.) auf Weizen (Triticum aestivum) anhand von Keimporenmerkmalen der Urediniosporen
A simple and fast light-microscopical method to identify rust species (Puccinia spp.) on wheat (Triticum aestivum) using germ pore features of urediniospores
Journal für Kulturpflanzen, 72 (2-3). S. 33–39, 2020, ISSN 1867-0911, DOI: 10.5073/JfK.2020.02-03.01, Verlag Eugen Ulmer KG, Stuttgart
 Dies ist ein Open-Access-Artikel, der unter den Bedingungen der Creative Commons Namensnennung 4.0 International Lizenz (CC BY 4.0) zur Verfügung gestellt wird (https://creativecommons.org/licenses/by/4.0/deed.de).
Dies ist ein Open-Access-Artikel, der unter den Bedingungen der Creative Commons Namensnennung 4.0 International Lizenz (CC BY 4.0) zur Verfügung gestellt wird (https://creativecommons.org/licenses/by/4.0/deed.de).In Mitteleuropa sind auf Weizen (Triticum aestivum) drei Rostpilzarten (Pucciniales) bekannt, nämlich der Schwarzrost (Puccinia graminis), der Gelbrost (P. striiformis) und der Braunrost (P. triticina). Diese Arten sind ökonomisch bedeutend. Um sie zu überwachen, frühzeitig zu erkennen und Ernteeinbußen zu minimieren, ist eine schnelle und korrekte Bestimmung der Pilzarten nötig. Hier wurde eine einfache lichtmikroskopische Methode optimiert und getestet, bei der Keimporenmerkmale der Urediniosporen zur Artdifferenzierung herangezogen werden. Die Methode lässt eine eindeutige Bestimmung zu. Die Ergebnisse werden mit Sequenzanalysemethoden in Bezug auf Bestimmungssicherheit, Zeitaufwand und Materialkosten verglichen.
Stichwörter: Pucciniales, Puccinia graminis, P. triticina, P. striiformis, Phasenkontrastmikroskopie, Artidentifizierung, Keimporenmerkmale, Sequenzanalyse, Methodenvergleich
In Central Europe there are three wheat rusts (Pucciniales) all of which are economically important. These are the (black) stem rust or wheat stem rust (Puccinia graminis), the leaf rust (P. triticina) and the stripe rust (P. striiformis). In order to monitore or control them effectively, efficient and reliable identification methods are needed. Here, a simple light-microscopical (phase contrast) method using germ pore features of urediniospores for identification is presented. This method makes it possible to identify the rust species exactly. In the present study this method is compared with the ITS sequence analyses with respect to identification accuracy, time and material costs.
Key words: Pucciniales, Puccinia graminis, P. triticina, P. striiformis, phase contrast microscopy, germ pore features, species identification, sequence analyses, method comparison
Rostpilze (Pucciniales) sind bedeutende Schadorganismen in der Landwirtschaft und können große Ernteeinbußen hervorrufen (z.B. Liebenberg und Pretorius, 2010, Huerta-Espino et al., 2011, Wellings, 2011). Die wirtschaftlich bedeutendsten durch Rostpilze verursachten Krankheiten an Weizen werden durch den Schwarzrost (P. graminis Pers.), den Gelbrost (P. striiformis Westend.) und den Braunrost (P. triticina Erikss.) hervorgerufen (Figueroa et al., 2018). Diese drei Arten sind auch aus Mitteleuropa bekannt (Gäumann, 1959, Klenke und Scholler, 2015). Am Landwirtschaftlichen Technologiezentrum Augustenberg (LTZ) werden besonders häufig Proben des Braun- und des Gelbrosts aus Baden-Württemberg zur Bestimmung eingereicht. Seit einem epidemischen Auftreten 2013 in Deutschland (Olivera-Firpo et al., 2017) steht zudem der Schwarzrost unter besonderer Beobachtung. Als extrem virulent gilt die Rasse Ug99, die sich seit 1998 von Uganda Richtung Norden und damit Richtung Europa ausbreitet (Singh et al., 2015, RustTracker.org, 2019). Auf dem Weizen, dem Telienwirt (Hauptwirt), werden drei Sporenstadien gebildet. Dies sind zunächst die Uredinien oder Uredolager (mit Urediniosporen), die bereits im Mai gebildet werden können. Es folgen im Sommer die dunklen Telien (mit Teliosporen). Schließlich keimen im Frühjahr des darauffolgenden Jahres Basidien (mit Basidiosporen) auf den vorjährigen abgestorbenen Blättern und Stängeln, die einen Aecienwirt infizieren können). Zur asexuellen Verbreitung der Rostpilze des Weizens dienen Urediniosporen, die in großer Menge gebildet werden. Diese können durch Wind über mehrere hundert Kilometer verbreitet werden (Roelfs, 1985; Nagarajan und Singh, 1990). Um Ernteausfälle zu minimieren und rechtzeitig angemessene und gezielte Bekämpfungsmaßnahmen zu ergreifen, ist eine schnelle und zuverlässige Identifizierung der Rostpilzarten anhand ihrer Urediniosporen nötig. Eine rein makroskopische Bestimmung der Arten anhand der Befallssymptome wäre eine schnelle Methode. Diese Methode ist jedoch bei Befall der Getreidepflanzen im Frühstadium unsicher bis unzureichend, da die typische Symptomausprägung erst im zeitlich fortgeschrittenen Zustand und bei stärkerem Befall zu erkennen ist (Blumer, 1963). So ist beispielsweise beim Gelbrost anfangs die arttypische Anordnung der Uredinien in Reihen noch nicht erkennbar. Beim Schwarzrost tritt der typische Befall des Stängels ebenfalls erst im fortgeschrittenen Infektionsprozess auf (Gäumann, 1959). Ganz allgemein werden makroskopische Merkmale von Weizen-Rostpilzen in Bestimmungsschlüsseln – da unsicher – nicht berücksichtigt (Cummins, 1971, Gäumann, 1959, Klenke und Scholler, 2015) Auch die mikroskopisch-morphologische Bestimmung, bei der häufig von in Wasser präparierten Sporen biometrische Daten (Sporenlänge und -breite, Form, Wanddicke) zur Unterscheidung herangezogen werden, ist zeitaufwändig und nur mit reifen, d.h. morphologisch voll ausgebildeten Urediniosporen möglich. Eine heute gängige Bestimmungsmethode ist die Sequenzanalyse. Bei Rostpilzen auf Gräsern wird die ITS Region (Internal Transcribed Spacer) eingesetzt und ermöglicht eine sichere Artbestimmung (Abbasi et al., 2005, Kuzdraliński et al., 2017, Liu und Hambleton, 2010, Barnes und Szabo, 2007, Fraaije et al., 2001). Dieses Verfahren, das auch am LTZ eingesetzt wird, ist jedoch relativ zeit- und kostenintensiv.
Anzahl und Verteilung der Keimporen der Urediniosporen bei Rostpilzen auf Gräsern sind bereits von Cummins (1956) als wichtiges Bestimmungs- und Artmerkmal bei Grasrosten erkannt worden. In diesem Beitrag testen wir mit dem Ziel der schnellen Artbestimmung Keimporenmerkmale mit Hilfe eines einfachen lichtmikroskopischen Phasenkontrastverfahrens, das bereits bei anderen Rostpilzgruppen (Scholler et al., 2014, Bubner et al., 2019) erfolgreich eingesetzt wurde. Diese Methodik wurde am Beispiel der Rostpilze des Weizens in Bezug auf Bestimmungssicherheit, Zeitaufwand und Materialkosten untersucht und mit den Ergebnissen von ITS-Sequenzanalysen verglichen.
Belegmaterial von P. triticina und P. striiformis wurde dem LTZ von Weizenbeständen aus Baden-Württemberg im Frühsommer 2018 zur Bestimmung zugeschickt. Die untersuchten Belege wurden als Referenz-Material im Herbarium des Staatlichen Museums für Naturkunde Karlsruhe (KR) hinterlegt und mit einer Referenznummer versehen (Tab. 1). Für die lichtmikroskopischen Untersuchungen von P. graminis wurden ältere Belege aus öffentlichen Herbarien in Berlin (B) und Karlsruhe (KR) ausgewertet, teils auch von anderen Wirten, da nicht ausreichend geeignetes Material auf Triticum aestivum zur Verfügung stand (Tab. 1).
Tab. 1. Belegmaterial, Funddaten, Referenznummern
Pilzart | Wirtsart (Sorte) | Herkunft | Sammeldatum | Herbarnummer | GenBank-Nr. |
P. graminis Pers. | Secale cereale L. | DE, Mecklenburg-Vorpommern, Lancken-Granitz | 15.08.1991 | KR-M-0003108 | / |
P. graminis Pers. | Elymus repens (L.) Gould | DE, Nordrhein-Westfalen, | 14.10.1961 | KR-M-0027529 | / |
P. graminis Pers. | E. repens (L.) Gould | DE, Nordrhein-Westfalen, | 14.10.1961 | KR-M-0027525 | / |
P. graminis Pers. | Triticum aestivum L. | FI, Varsinais-Suomi, Tuorla | 21.08.1951 | B 700100001 | / |
P. graminis Pers. | Lolium perenne L. | DE, Baden-Württemberg, | 11.08.2005 | KR-M-0018541 | / |
P. striiformis Westend. | T. spelta L. | DE, Baden-Württemberg, Ladenburg | 08.05.2018 | KR-M-0006114 | MK880613 |
P. striiformis Westend. | T. aestivum L. (Zenon) | DE, Baden-Württemberg, Grötzingen | 18.05.2018 | KR-M-0006111 | MK880607 |
P. striiformis Westend. | T. dicoccon (Schrank) Schübl. (Ramses) | DE, Baden-Württemberg, Grötzingen | 18.05.2018 | KR-M-0006395 | MK880623 |
P. striiformis Westend. | T. aestivum L. | DE, Baden-Württemberg, Rotfelden | 17.05.2018 | KR-M-0006392 | MK880614 |
P. striiformis Westend. | T. aestivum L. (Akteur) | DE, Baden-Württemberg, Döggingen | 27.06.2018 | KR-M-0006404 | MK880609 |
P. triticina Erikss. | T. aestivum L. | DE, Baden-Württemberg, Stifterhof | 29.05.2018 | KR-M-0006391 | MK880610 |
P. triticina Erikss. | T. aestivum L. | DE, Baden-Württemberg, | 06.06.2018 | KR-M-0006389 | MK880612 |
P. triticina Erikss. | T. aestivum L. (Meister) | DE, Baden-Württemberg, Bönnigheim | 08.06.2018 | KR-M-0006388 | MK880617 |
P. triticina Erikss. | T. aestivum L. (Bernstein) | DE, Baden-Württemberg, Tailfingen | 08.06.2018 | KR-M-0006401 | MK880621 |
P. triticina Erikss. | T. aestivum L. (Faustus) | DE, Baden-Württemberg, Orschweier | 08.06.2018 | KR-M-0006399 | MK880615 |
P. triticina Erikss. | T. aestivum L. (Faustus) | DE, Baden-Württemberg, Orschweier | 12.06.2018 | KR-M-0006397 | MK880608 |
Die Keimporenmerkmale (Anzahl, Position) wurden mit geringen Abweichungen hinsichtlich der Trocknungszeit nach der Methode von Scholler et al. (2014) und Bubner et al. (2019) ausgewertet. Sporen aus einem Sorus eines Belegs (Tab. 1) wurden auf einen Objektträger in Hoyers Medium (Cunningham, 1972) überführt und bei 400-facher Vergrößerung und Phasenkontrast untersucht (Axioskop 2 Plus, Carl Zeiss, Oberkochen, Deutschland). Je Beleg wurden 25 Sporen ausgewertet. Gegebenenfalls wurden Sporen von zusätzlichen Sori pro Objektträgerpräparat verwendet, um die Sporendichte zu erhöhen und somit die Auswertungszeit zu minimieren. Die Auswertung erfolgte sofort (unmittelbar nach Herstellung des Objektträgerpräparats) und nach 6, 14, 20, 24, 42, 48 und 66 h im Trockner (bei jeweils 40°C). Fotos der Urediniosporen wurden mittels einer Jenoptik ProgRes CT3 Digitalkamera für Mikroskope und dem Programm PROGRES CAPTUREPRO Version 2.10.0.1 (Jenoptik, Jena, Deutschland) aufgenommen.
Proben aus Baden-Württemberg, bei denen nur ein Sporenstadium (Uredinien) vorlag, wurden zur Absicherung sequenziert. Dafür wurden je Blattprobe zwischen einem und drei Uredinien mit möglichst wenig anhängendem Pflanzenmaterial mittels Skalpell und Pinzette entnommen und in ein 1,5 ml-Reaktionsgefäß überführt. Die DNA wurde nach Herstelleranleitung mit dem DNeasy Plant Mini Kit (Qiagen, Hilden, Deutschland) extrahiert. Im Anschluss wurde die komplette ITS-Region der Rostpilze mit den rostpilzspezifischen Primern ITS1rustF10d (5´-TGAACCTGCAGAAGGATCATTA-´3, Barnes und Szabo, 2007) bzw. Rust2inv (5′-GATGAAGAACACAGTGAAA-´3, Aime, 2006) und ITS4 (5´-TCCTCCGCTTATTGATATGC-´3, White et al., 1990) amplifiziert (Liu und Hambleton, 2010). Die PCR wurde mit der HotStarTaq Polymerase (Qiagen, Hilden, Deutschland) wie folgt durchgeführt: Denaturierung 15 min bei 95°C, Amplifikation mit 40 Zyklen (15 sec 94°C, 30 sec 52°C für ITSgesamt bzw. 30 sec 50°C für ITS2, 40 sec 72°C) und letzte Extension 10 min 72°C.
Für die Sequenzierung wurden die rostpilzspezifischen PCR-Amplifikate (Rust2inv/ITS4) mit dem Wizard® SV Gel and PCR CleanUp System (Promega, Madison, Wisconsin, USA) gereinigt. Die Sequenzierreaktion wurde mit dem BigDye® Terminator v.1.1 Cycle Sequencing Kit angesetzt, anschließend mit dem DyeEx 2.0 Spin Kit (Qiagen) gereinigt und auf dem Applied Biosystems SeqStudio Genetic Analyzer (Thermo Fischer Scientific, Waltham, Massachusetts, USA) sequenziert. Die DNA-Sequenzen wurden mit der Lasergene-Software (DNASTAR, Madison, Wisconsin, USA) ausgewertet. Vorwärts- und Rückwärtstrang wurden zu einem Contig zusammengefügt und Kontrollgelesen. Anschließend wurden die erzeugten Sequenzdaten mit den Sequenzen der NCBI Genbank (National Center for Biotechnology Information) mittels BLAST-Funktion (Basic Local Alignment Search Tool) verglichen und identifiziert. Zur Kontrolle erfolgte ein zusätzlicher Vergleich der Sequenzen im BOLD-System (Ratnasingham und Hebert, 2007).
Die hier generierten Sequenzen wurden in der NCBI GenBank (https://www.ncbi.nlm.nih.gov/genbank/) hinterlegt.
Keimporenanzahl und -position waren in der Regel direkt nach der Präparatherstellung schlecht bis gar nicht erkennbar. Nach 6 h Trocknung war eine deutliche Verbesserung der Keimporensichtbarkeit zu sehen. Die Keimporen bei P. graminis und P. triticina waren nach dieser Zeit gut zu erkennen und somit die Arten sicher bestimmbar. Nach 24 h konnte noch eine zusätzliche Verbesserung der Keimporenschärfe festgestellt werden. Bei P. striiformis waren die Keimporen ohne Trocknung nicht erkennbar. Nach mindestens 20 h Trocknung waren die Keimporen sicher erkennbar, jedoch im Vergleich zu den anderen beiden untersuchten Arten nicht ganz so deutlich (Abb. 1 A, B). Nach 24 h konnte eine zusätzliche Verbesserung der Keimporensichtbarkeit festgestellt werden und es wurde gleichzeitig das Optimum erreicht. Bei P. striiformis kann die Sichtbarmachung zusätzlich durch Zerbrechen der Sporen und Herausdrücken des Plasmas (z.B. durch vorsichtiges Drücken auf das Deckplättchen mit einem Radiergummi) verbessert werden (Abb. 1 C).
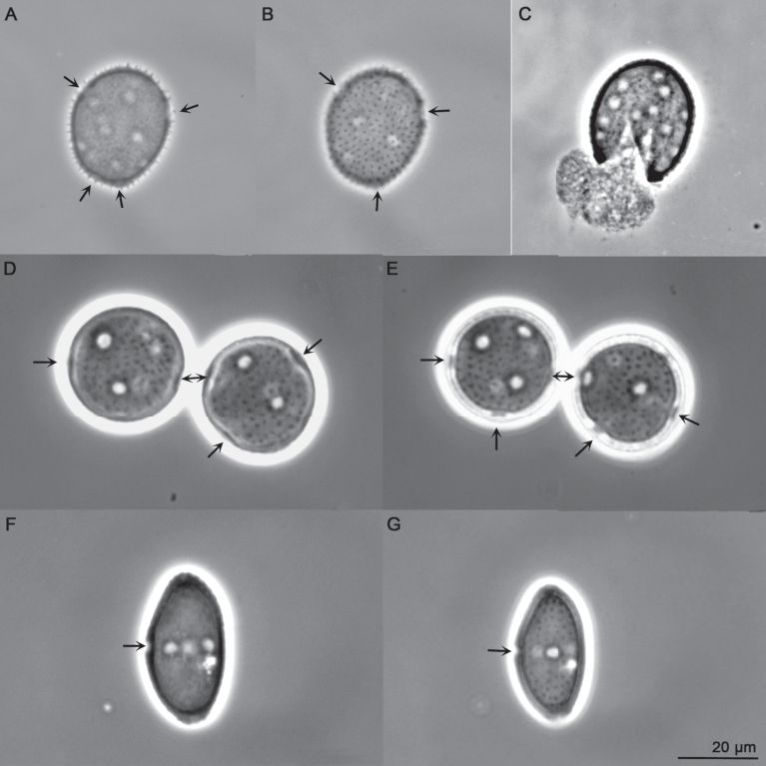
Abb. 1. Keimporen der Urediniosporen. A, B: Puccinia striiformis, in zwei Schärfeebenen. C: P. striiformis, Spore plasmafrei. D, E: P. triticina in zwei Schärfeebenen. F, G: P. graminis in zwei Schärfeebenen. Die Keimporen sind in der Aufsicht als weiße Kreise erkennbar und in der Seitenansicht durch Pfeile gekennzeichnet.
Die für die drei Arten ermittelten Keimporenmerkmale stimmen weitgehend mit denen von Cummins (1971) überein. Die Urediniosporen waren somit klar jeweils einer Art zuzuordnen. Die Keimporen von P. triticina und P. striiformis sind zerstreut, die von P. graminis äquatorial angeordnet (Abb. 1 F, G). In den folgenden Angaben zur Keimporenzahl sind unsere Werte außerhalb des 80%-Perzentils in Klammern gesetzt, die Werte in Klammern bei Cummins (1971) entsprechen dagegen keinen statistisch definierten Werten. Die Keimporenzahl beträgt bei P. striiformis (7) 9–12 (14) (Median 10), bei P. triticina (6) 7–9 (10) (Median 8) und bei P. graminis (3) 4–5 (6) (Median 4) (Abb. 2).
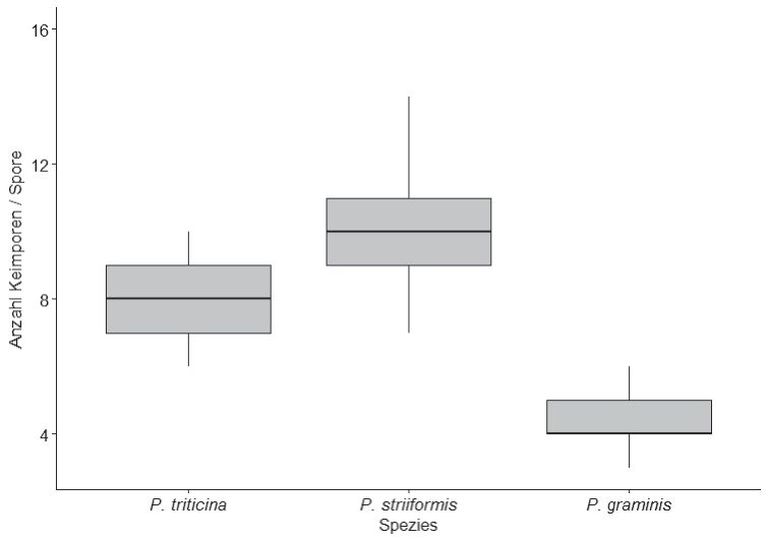
Abb. 2. Boxplot der Keimporenanzahl pro Spore von Puccinia triticina (n = 6), P. striiformis (n = 5) und P. graminis (n = 5). Dargestellt sind Median, „Whisker“ und Quantile.
1 Keimporen äquatorial, |
P. graminis |
1* Keimporen zerstreut, |
2 |
2 Keimporenzahl meist 7–9 |
P. triticina |
2* Keimporenzahl meist 9–12 |
P. striiformis |
Die GenBank-Eingangsnummern sind in Tabelle 1 aufgelistet. Die Analyse der rostpilzspezifischen ITS-Sequenzen durch BLAST-Vergleich mit bereits in GenBank und BOLD hinterlegten Sequenzen bestätigt die Artzuordnung der morphologischen Bestimmung. Bei zwei Belegen, die mit allgemeinen ITS-Primern sequenziert wurden, ergab die Sequenzanalyse statt der Rostpilz-DNA die DNA eines anderen Pilzes (Kontamination). Diese Belege wurden nicht für die Auswertung berücksichtigt.
Der zeitliche Aufwand pro Probe betrug für die mikroskopische Präparation mindestens 3 min, für die Trocknung des Objektträgerpräparats 6 bis 20 h (Optimum 24 h) und für die Auswertung im Durchschnitt 18 min. Somit lag der gesamte Zeitaufwand bei ca. 20 h und 21 min. Bei der Untersuchung von mehr Proben erhöht sich entsprechend die benötigte Zeit für die Auswertung und Präparatherstellung pro zusätzlicher Probe um 21 Minuten.
Bei der Sequenzierung betrug der zeitliche Aufwand pro Probe ca. 8 h, davon wurden ca. 3 h für Pipettierarbeiten, Gerätebedienung im Labor und Auswertungen benötigt, die restliche Zeit waren Wartezeiten, d.h. Laufzeiten der Geräte (Schütteln bei der DNA-Isolierung, PCR-Lauf, Sequenzierreaktion, Sequenzierlauf auf dem Sequenzer). Es wurden meistens mehrere Proben parallel bearbeitet, daher erhöhte sich nur die Zeit für die Laborarbeit und Auswertung um ca. 50%, Die Laufzeiten der Geräte blieben dieselben. Sollten die PCR-Produkte an ein externes Labor zur Sequenzierung weggeschickt werden, verlängert sich die Wartezeit auf die DNA-Sequenzen auf 1–3 Tage.
Der Materialaufwand für die lichtmikroskopische Bestimmung pro Probe beinhaltet Hoyers Medium, einen Objektträger und ein Deckblättchen und kostet 9 Cent.
Im Vergleich zur Mikroskopie ist der Materialaufwand bei der molekularbiologischen Untersuchung viel höher. Es werden mehrere Reagenzien und Einwegmaterialien wie Pipettenspitzen, Reagenzgefäße etc. benötigt. Die Gesamtkosten für eine Sequenzanalyse mit DNA-Isolierung und PCR liegen bei ca. 45 €/Probe (DNA-Isolierung plus PCR liegt bei ca. 12 €/Probe). Die Ergebnisse sind in Tabelle 2 zusammengefasst.
Tab. 2. Vergleich zweier Methoden zur Frühbestimmung von in Deutschland vorkommenden Rostpilzen auf Weizen
| Morphologische Bestimmung (Keimporenmerkmale) | Sequenzierung (ITS) |
Artbestimmung bei reifen Urediniosporen | gut | gut |
Artbestimmung bei geschlossenen Sori mit unreifen Urediniosporen | schlecht | gut |
Fehlbestimmungen | nein | möglich (bei Sequenzierung mit allgemeinen ITS-Primern) |
Materialkosten | gering | hoch |
Zeitaufwand | ≤ 20,5 h (reine Bearbeitung | 8 h (reine Bearbeitungszeit ca. 3 h) |
Geräte | Lichtmikroskop mit Phasenkontrast, Stereomikroskop, Trockenschrank | Zentrifuge, Thermocycler, Sequenziergerät, PC |
Sonstiges |
| Sequenzdaten |
Aufgrund der großen ökonomischen Relevanz der Getreideroste wurden internationale Initiativen wie die Borlaug Global Rust Initiative (www.globalrust.org) oder das Global Cereal Rust Monitoring System (GCRMS) etabliert (Park et al., 2011). Sie sollen unter anderem das weltweite Auftreten von Weizengelb-, -braun- und -schwarzrost kontrollieren und überwachen sowie geeignete Gegenmaßnahmen entwickeln, um die Lebensmittelversorgung weltweit zu sichern. Die Resistenzzüchtung ist durch das immer wieder neue Auftreten von Rostpilzrassen eine langfristige Aufgabe. Da die Resistenz von Sorten durch neue, virulente Rostrassen zum Teil sehr schnell überwunden werden kann, ist der Anbau resistenter Sorten als alleinige Schutzmaßnahme nicht ausreichend (Kolmer, 2005). Daher sind die Überwachung der Schaderreger und ein gezielter Fungizideinsatz im Infektionsfall nötig.
Mit der weiterentwickelten Methode nach Cunningham (1972), Scholler et al. (2014) und Bubner et al. (2019) kann eine sichere Bestimmung der Rostpilzarten auf Weizen gewährleistet werden. Sie ist nach unserer Erfahrung robuster als die Sequenzierung mit allgemeinen ITS-Primern, da immer wieder kleinste Verunreinigungen zur Sequenzierung anderer Pilzarten führen können. Diese Sequenzen können dann nicht verwendet werden. Die mikroskopische Methode hingegen ermöglicht es, bei einem Mischpräparat mit mehreren Pilzarten direkt anhand der Sporen eine irrelevante Pilzart (z.B. Schimmelsporen) während der Auswertung zu ignorieren und speziell die Rostpilzsporen zu analysieren. Ein weiteres wichtiges, wenn nicht sogar das wichtigste Kriterium ist der zeitliche Aufwand für die Bearbeitung. Bei Verwendung einer adäquaten Sporenmenge pro Objektträgerpräparat, errechnet sich ein Zeitaufwand von ca. 20 h 21 min je Probe (Bearbeitungszeit 21 min pro Probe). Die Sequenzanalyse erfordert am LTZ etwa 8 Stunden bei einer Bearbeitungszeit von 3 h (Tab. 2). Klar im Vorteil ist die Keimporenanalyse in Bezug auf Sachmittelkosten. Während Sequenzanalysen 45 €/Probe erfordern, liegen die Sachkosten bei Lichtmikroskopie bei 9 Cent. Ungünstig für die Keimporenuntersuchungen sind sehr frühe Befallssymptome, wenn die Epidermis die Sori noch überdeckt. In diesem Zustand sitzen die Urediniosporen noch auf Stielen und haben noch nicht ihre arttypischen morphologischen Merkmale entwickelt. Selbst bei P. graminis und P. triticina sind die Keimporen dann noch nicht erkennbar. Dies zeigt, dass die Keimporenanalyse erst dann beginnen kann, wenn bei einer Rostpilz-Probe bei einem Sorus die Epidermis aufgerissen ist. Dies spielt bei der Sequenzanalyse keine Rolle. Die in dieser Arbeit zur Keimporenuntersuchung verwendete Methode muss, wie auch schon in vorherigen Publikationen gezeigt (Scholler et al., 2014, Bubner et al., 2019), für jede Pilzgruppe gesondert optimiert werden. Dies ist jedoch bei den Rostpilzen des Weizens der Gattung Puccinia einfach.
Die morphologische Methode basierend auf Keimporenmerkmalen ist der molekularen Analyse unter bestimmten Voraussetzungen überlegen. Die Bestimmung ist problemlos möglich und Fehler durch Verunreinigungen, die hin und wieder bei Sequenzanalysen auftreten, können bei der morphologischen Analyse ausgeschlossen werden. Zudem ist der Materialaufwand deutlich geringer. Lediglich bei sehr jungen Befallssymptomen (noch von der Epidermis geschlossene Sori mit unreifen Urediniosporen) sollte sequenziert werden, da hier morphologische Differentialmerkmale für die Bestimmung nicht ausreichend sind. Somit kann die molekularbiologische Methode früher in der Krankheitsentwicklung eingesetzt werden als die morphologische Methode. Insgesamt gesehen, ergänzen sich beide Methoden jedoch sinnvoll. Insbesondere bei der Absicherung von Untersuchungsergebnissen ist der Einsatz zweier auf unterschiedlichen Prinzipien (molekularbiologisch, morphologisch) beruhenden Nachweisverfahren geboten.
Wir danken Herrn Dr. Robert Lücking (Herbarium B) für die Ausleihe von Puccinia graminis-Belegen auf Triticum aestivum. Unser Dank gilt auch Dr. Josef Simmel und Dr. Wolfgang Maier für die Durchsicht des Manuskripts und die wertvollen Hinweise.
Die Autoren erklären, dass keine Interessenskonflikte vorliegen.
Abbasi, M., S.B. Goodwin, M. Scholler, 2005: Taxonomy, phylogeny and origin of Puccinia graminis, the black stem rust: new insights based on rDNA sequence data. Mycoscience 46, 241-247, DOI: 10.1007/s10267-005-0244-x.
Aime, M.C., 2006: Toward resolving family-level relationships in rust fungi (Uredinales). Mycoscience 47, 112–122, DOI: 10.1007/s10267-006-0281-0.
Barnes, C.W., L.J. Szabo, 2007: Detection and identification of four common rust pathogens of cereals and grasses using real-time polymerase chain reaction. Phytopathology 97 (6), 717–727, DOI: 10.1094/PHYTO-97-6-0717.
Blumer, S., 1963: Rost- und Brandpilze auf Kulturpflanzen. Ein Bestimmungsbuch für die in Mitteleuropa vorkommenden Arten. Jena, G. Fischer (Abb. 36, S. 142).
Bubner, B., R. Buchheit, F. Friedrich, V. Kummer, M. Scholler, 2019: Species identification of European forest pathogens of the genus Milesina (Pucciniales) using urediniospore morphology and molecular barcoding including M. woodwardiana sp. nov. MycoKeys 48, 1-40, DOI: 10.3897/mycokeys.48.30350.
Cummins, G.B., 1956: Host index and morphological characterization of the grass rusts of the world. Plant Disease Reporter Suppl. 237, 1-52.
Cummins, G.B., 1971: The rust fungi of cereals, grasses and bamboos. Berlin, Heidelberg, New York, Springer.
Cunningham, J.L., 1972: A miracle mounting fluid for permanent whole-mounts of microfungi. Mycologia 64, 906-911.
Figueroa, M., K.E. Hammond-Kosack, P.S. Solomon, 2018: A review of wheat diseases-a field perspective. Molecular Plant Pathology 19 (6), 1523–1536, DOI: 10.1111/mpp.12618.
Fraaije, B.A., D.J. Lovell, J.M. Coelho, S. Bladwin, D.W. Hollomon, 2001: PCR-based assays to assess wheat varietal resistance to blotch (Septoria tritici and Stagonospora nodorum) and rust (Puccinia striiformis and Puccinia recondita) diseases. European Journal of Plant Pathology 107, 905-917.
Gäumann, E,., 1959: Die Rostpilze Mitteleuropas. Beiträge zur Kryptogamenflora der Schweiz 12. Büchler & Co, Bern.
Huerta-Espino, J., R.P. Singh, S. Germán, B.D. McCallum, R.F. Park, W.Q. Chen, S.C. Bhardwaj, H. Goyeau, 2011: Global status of wheat leaf rust caused by Puccinia triticina. Euphytica 179, 143-160.
Klenke, F., Scholler, M., 2015: Pflanzenparasitische Kleinpilze. Berlin, Heidelberg, Spriner, DOI: 10.1007/978-3-662-46162-4.
Kolmer, J.A., 2005: Tracking wheat rust on a continental scale. Current Opinion in Plant Biology 8, 441-449, DOI: 10.1016/j.pbi.2005.05.001.
Kuzdraliński, A., A. Kot, H. Szczerba, A. Ostrowska, M. Nowak, M. Muszyńska, M. Lechowski, P. Muzyka, 2017: Novel PCR assays for the detection of biological agents responsible for wheat rust diseases: Puccinia triticina and Puccinia striiformis f. sp. tritici. Journal of Molecular Microbiology and Biotechnology 27 (5), 299-305.
Liebenberg, M.M., Z.A. Pretorius, 2010: Common bean rust: pathology and control. In: Horticultural Reviews. Janick, J.(Hrsg.). Hoboken, NJ, Wiley-Blackwell, S.1-99.
Liu, M., S. Hambleton, 2010: Taxonomic study of stripe rust, Puccinia striiformis sensu lato, based on molecular and morphological evidence. Fungal Biology 114 (10), 881-899.
Nagarajan, S., D.V. Singh, 1990: Long-distance dispersion of rust pathogens. Annual Review of Phytopathology 28, 139-153.
Olivera-Firpo, P.D., M. Newcomb, K. Flath, N. Sommerfeldt-Impe, L. Szabo, M. Carter, D.G. Luster, Y. Jin, 2017: Characterization of Puccinia graminis f. sp. tritici isolates derived from an unusual wheat stem rust outbreak in Germany in 2013. Plant Pathology 66, 1258–1266, DOI: 10.1111/ppa.12674.
Park, R., T. Fetch, D. Hodson, Y. Jin, K. Nazari, M. Prashar, Z. Pretorius, 2011: International surveillance of wheat rust pathogens: progress and challenges. Euphytica 179 (1), 109–117, DOI: 10.1007/s10681-011-0375-4.
Ratnasingham, S., P.D.N. Hebert, 2007: BOLD: The Barcode of Life Data System (www.barcodinglife.org). Molecular Ecology Notes 7, 355-364, DOI: 10.1111/j.1471-8286.2007.01678.x.
Roelfs, A.P., 1985: Wheat and rye steam rust. In: The cereal rusts. Vol. II. Roelfs, A. P., W. R. Bushnell (Hrsg.), Orlando, Academic Press INC,.
Scholler, M., M. Abbasi, F. Friedrich, 2014: Tranzschelia in the Americas revisited: two new species and notes on the Tranzschelia thalictri complex. Mycologia 106, 448–455, DOI: 10.3852/12-260.
Singh, R.P., D.P. Hodson., Y. Jin, E.S. Lagudah, M.A. Ayliffe, S. Bhavani, M.N. Rouse, Z.A. Pretorius, L.J. Szabo, J. Huerta-Espino, B.R. Basnet, C.X. Lan, M.S. Hovmøller, 2015: Emergence and spread of new races of wheat stem rust fungus: continued threat to food security and prospects of genetic control. Phytopathology 105, 872–884, DOI: 10.1094/PHYTO-01-15-0030-FI.
RustTracker.org, 2019: A global wheat rust monitoring system. Zugriff 2.12.2019. https://rusttracker.cimmyt.org/?page_id=22.
Wellings, C.R., 2011: Global status of stripe rust: a review of historical and current threats. Euphytica 179, 129-141, DOI: 10.1007/s10681-011-0360-y.
White, T.J., T. Bruns, S. Lee, J. Taylor, 1990: Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenies. In: PCR Protocols A Guide to Methods and Applications. Innis, M. A., D. H. Gelfand, J. J. Sninsky, T. J. White (Hrsg.),: San Diego, Academic Press, S. 315-322.